ОЦЕНКА ЭФФЕКТИВНОСТИ И БЕЗОПАСНОСТИ ПРИМЕНЕНИЯ 1,8% БИОРЕВИТАЛИЗАНТА ДЛЯ КОРРЕКЦИИ ИНВОЛЮЦИОННЫХ ИЗМЕНЕНИЙ ЛИЦА
13.09.2023
Борзых Ольга Борисовна
К.м.н., врач-дерматовенеролог, научный сотрудник ЦКП «Молекулярные и клеточные технологии», косметолог, клиника пластической хирургии и косметологии «Доктор Альбрехт», Воронеж
Актуальность усовершенствования методов коррекции инволюционных изменений кожи лица связана с несколькими причинами. Так, в связи с увеличением ожидаемой продолжительности жизни количество пациентов с инволюционными изменениями кожи неуклонно растет. При этом пациенты стремятся как можно дольше сохранять свою социальную активность. Одной из функций кожи, как известно, является социальная; состояние кожи помогает окружающим людям сложить о нас то или иное впечатление. Таким образом, максимально долгое поддержание функций кожи, в том числе и социальной, является одной из приоритетных задач эстетической медицины [1].
Известно множество факторов, влияющих на старение кожи. В основе патогенеза этого процесса лежит снижение синтетической активности фибробластов, которое приводит к нарушению структуры и свойств внеклеточного матрикса кожи. В свою очередь, известно, что внеклеточный матрикс кожи имеет не только опорную функцию, но и функцию участия в синтетических и пролиферативных процессах в коже. Нарушение строения внеклеточного матрикса кожи вызывает нарушение функций. Таким образом реализуется порочный круг: снижение синтетической активности фибробластов способствует нарушению строения и функционирования внеклеточного матрикса кожи, что еще больше нарушает синтетическую активность фибробластов [2–8].
В эстетической медицине существует большое количество хирургических и нехирургических способов коррекции возрастных изменений. Нехирургические методы остаются наиболее популярными по причине малой травматичности и большей безопасности в сравнении с хирургическими методами. В свою очередь, среди нехирургических не все методы обладают патогенетически обоснованным воздействием на инволюционные изменения кожи. Так, например, заполнение складок препаратами для контурной пластики лишь восполняет потерянный объем, практически не влияя на состояние дермы [9–11].
Среди препаратов, оказывающих патогенетически обоснованное воздействие на инволюционные изменения кожи, «золотым стандартом» остается биоревитализация. Действие гиалуроновой кислоты (ГК) основано на создании во внеклеточном матриксе условий для работы фибробластов. В результате повышается синтетическая активность фибробластов, что проявляется повышением экспрессии генов коллагена I типа и эластина [1, 12–14].
В настоящее время существует большое число биоревитализантов как на основе чистой ГК, так и с добавлением различных биологически активных компонентов. Однако, как правило, препараты с комплексным составом имеют более высокую стоимость, а при выборе средства для биоревитализации врач-косметолог всегда учитывает и экономическую целесообразность применения того или иного препарата. Таким образом, целью исследования была оценка клинической эффективности и безопасности применения нативной ГК при коррекции инволюционных изменений кожи.
Материал и методы
Простое слепое рандомизированное плацебо-контролируемое исследование было проведено на базе Центра коллективного пользования «Молекулярные и клеточные технологии» ФГБОУ ВО КрасГМУ им. проф. В.Ф. Войно-Ясенецкого Минздрава России (Красноярск) и клиники пластической хирургии и косметологии «Доктор Альбрехт» (Воронеж) в 2021–2022 гг. В исследование были включены 45 женщин со средней степенью выраженности возрастных изменений лица (индекс инволюционных изменений до 21) [15].
Критерии включения: соматически и дерматологически здоровые женщины в возрасте от 35 до 45 лет включительно, не имевшие в анамнезе косметологических процедур в течение года перед включением в исследование, гормональных нарушений, выраженного фотостарения и не принимавшие лекарственных препаратов, влияющих на состояние кожи.
Исследование было одобрено локальным этическим комитетом (ЛЭК) РНИМУ им. Н.И. Пирогова № 206 от 22.03.2021, все пациентки подписывали информированное добровольное согласие на исследование и фотодокументирование.
Все пациентки были разделены на 2 группы в зависимости от используемого препарата. В основную группу вошли 25 женщин (средний возраст 39,9 ± 3,03 года), которым было проведено внутрикожное инъецирование биоревитализанта Hyon 1,8%, 3 процедуры, с интервалом 14–20 дней.
Препарат Hyon 1,8% («Инфарм», Россия, РУ № РЗН 2018/7614) произведен на основе нативной (неретикулированной) ГК, концентрация ГК — 18 мг/мл.
В группу сравнения вошли 20 женщин (средний возраст 40,5 ± 2,96 года), которым было проведено внутрикожное инъецирование плацебо (физиологический раствор), 3 процедуры, с интервалом 14–20 дней.
Клиническая эффективность проведенных процедур оценивалась на основе анализа опросников пациентов: валидированная международная глобальная шкала эстетического улучшения (Global Aesthetic Improvement Scale; GAIS) и невалидированная (разработанная авторами), учитывающая оценку изменения различных показателей кожи.
По шкале GAIS результаты оцениваются от 5 баллов, что соответствует «ухудшению внешнего вида», до 1 балла, что соответствует «выраженному улучшению».
Изменение отдельных качественных показателей кожи пациентки оценивали по разработанной нами шкале, при этом отсутствие изменений оценивалось в 0 баллов, невыраженное изменение — в 1 балл, выраженное изменение — в 2 балла.
Также эффективность процедур оценивалась по динамике толщины кожи до и после процедур по данным ультразвуковой (УЗ) сонографии в 6 точках измерения: в средней трети лица, в нижней трети лица и в субментальной области справа и слева в каждом случае. Показатели, зарегистрированные при УЗ-сонографии в субментальной области, где внутридермальные инъекции не проводились, использовали в качестве контроля.
Для оценки морфологических изменений кожи проводилось гистологическое исследование биоптатов кожи, которые были взяты в околоушной области, где дополнительно были проведены внутрикожные инъекции препаратов до проведения процедур и через 30 дней после последней инъекции.
Оценка безопасности процедуры проводилась путем регистрации нежелательных явлений (НЯ) после процедуры.
Статистическая обработка результатов проводилась с использованием пакета программ для медицинских исследований Jamovi. Для определения достоверности результатов использовали критерий Манна – Уитни (для независимых выборок), критерий Уилкоксона (для парных выборок). Различия считались статистически достоверными при p < 0,05.
Результаты и обсуждение
Клиническая эффективность
По шкале GAIS все пациентки из основной группы отметили улучшение качества кожи после применения препарата Hyon 1,8% (рис. 1, 2). При этом 48% пациенток указали, что имеется выраженное улучшение, при котором не требовалась дополнительная коррекция возрастных изменений.
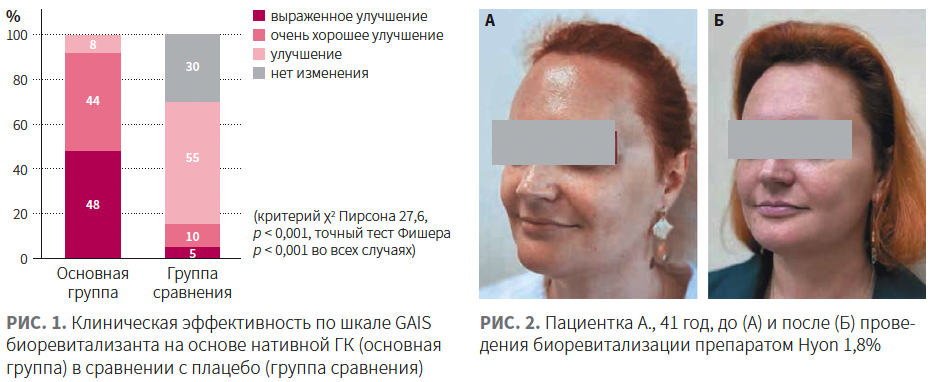
По результатам анкетирования, изменение цвета кожи, улучшение сияния, увеличение увлажненности, смягчение кожи, повышение тонуса, сужение расширенных пор и уменьшение выраженности мелких морщин были статистически значимо более выраженны в основной группе пациенток после биоревитализации Hyon 1,8% в сравнении с группой пациенток после применения плацебо. Более всего изменились следующие показатели: увлажненность кожи, изменение цвета и повышение мягкости кожи (улучшение тактильных ощущений) (табл. 1).
Таблица 1. Результаты анкетирования пациенток по шкале изменения состояния кожи после внутрикожного инъецирования биоревитализанта на основе нативной ГК (основная группа) или плацебо (группа сравнения)
|
Параметры кожи, баллы |
Основная группа |
Группа сравнения |
|
Цвет |
1,55 ± 0,510 |
0,600 ± 0,598* |
|
Сияние |
1,29 ± 0,464 |
0,150 ± 0,366* |
|
Увлажненность |
1,64 ± 0,490 |
0,650 ± 0,489* |
|
Мягкость |
1,54 ± 0,509 |
0,650 ± 0,489* |
|
Расширенные поры |
1,13 ± 0,743 |
0* |
|
Тонус кожи |
1,42 ± 0,504 |
0,263 ± 0,452* |
|
Мелкие морщины |
1,38 ± 0,590 |
0* |
Примечание. * — р < 0,001.
Результаты УЗ-сонографии
У пациенток основной группы после применения биоревитализанта на основе нативной ГК Hyon 1,8% было отмечено статистически значимое увеличение толщины кожи в области средней и нижней третей лица. Не зарегистрировали статистически значимого увеличения толщины кожи в субментальной области у пациенток из основной группы и во всех точках у пациенток из группы плацебо (табл. 2, 3).
Таблица 2. Толщина кожи по данным УЗ-сонографии в основной группе пациенток до и после внутрикожного инъецирования препарата на основе нативной ГК (n = 25)
|
Область лица |
До |
После |
|
Средняя треть лица |
1,95 ± 0,206 |
2,80 ± 0,384* |
|
Нижняя треть лица |
1,62 ± 0,250 |
2,2 ± 0,364* |
|
Субментальная область |
1,37 ± 0,144 |
1,36 ± 0,150 |
Примечание. * — р < 0,001.
Таблица 3. Динамика толщины кожи у пациенток основной группы и группы сравнения: изменение толщины по данным УЗ-сонографии, %
|
Область лица |
Основная группа |
Группа сравнения |
|
Средняя треть лица |
44,0 ± 14,3* |
0,156 ± 3,35 |
|
Нижняя треть лица |
36,5 ± 11,1* |
–0,647 ± 4,37 |
|
Субментальная область |
–0,570 ± 6,21 |
–0,283 ± 5,61 |
Примечание. * — р < 0,001.
Результаты гистологического исследования
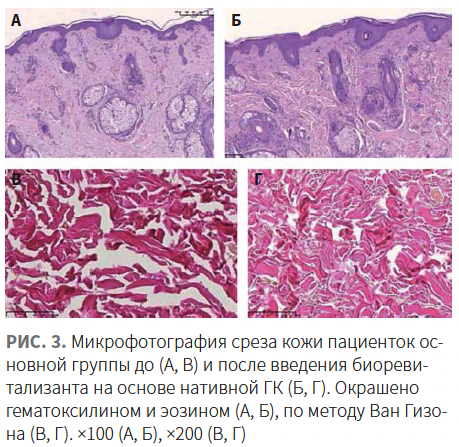
У пациенток группы сравнения после инъецирования физиологического раствора в качестве плацебо значимых морфологических изменений отмечено не было.
После применения нативной ГК (Hyon 1,8%) наблюдались выраженные структурные изменения. В микросрезах отмечено утолщение эпидермиса, преимущественно за счет шиповатого слоя, увеличение толщины сосочкового слоя дермы (рис. 3А, Б). В сосочковом слое было отмечено повышение плотности клеточных элементов. В сетчатом слое визуализировались крупные пучки коллагеновых волокон (рис. 3В, Г).
После применения нативной ГК морфологические изменения сосочкового и сетчатого слоя дермы могут быть обусловлены созданием благоприятной для синтеза среды для фибробластов (с повышением сигналинга), а изменения эпидермиса — улучшением кровоснабжения дермы и доставки питательных веществ к эпидермису через дермо-эпидермальную границу.
Результаты оценки безопасности
Зарегистрировали следующие НЯ:
- всех пациенток покраснение кожи сразу после процедуры, самостоятельно разрешающееся в течение 1–2 ч;
- у всех пациенток отечность кожи после процедуры, самостоятельно разрешающаяся в течение суток;
- петехии после 50 (66,67%) процедур у пациенток основной группы и 36 (60%) процедур у пациенток группы сравнения.
В течение всего исследования нами не были отмечены НЯ, требующие вмешательства врача для их разрешения.
Заключение
Проведенное нами исследование показало высокую клиническую эффективность и безопасность применения препарата Hyon 1,8% для биоревитализации. В сравнении с результатами применения плацебо отмечены улучшение всех основных качественных характеристик кожи, высокая удовлетворенность результатами процедур.
Результаты клинической оценки получили подтверждение при проведении УЗ-сонографии кожи. Так, после применения препарата Hyon 1,8% было зафиксировано увеличение толщины кожи в области средней и нижней третей лица. Данные гистологического исследования продемонстрировали морфологические изменения, лежащие в основе клинических результатов применения препарата Hyon 1,8%.
Литература
- Ganceviciene R., Liakou A.I., Theodoridis A., et al. Skin anti-aging strategies. Dermatoendocrinol 2012; 4(3): 308–319.
- Humphrey S., Manson Brown S., Cross S.J., Mehta R. Defining Skin Quality: Clinical Relevance, Terminology, and Assessment. Dermatol Surg 2021; 47(7): 974–981.
- Low E., Alimohammadiha G., Smith L.A., et al. How good is the evidence that cellular senescence causes skin ageing? Ageing Res Rev 2021; 71: 101456.
- Farage M.A., Miller K.W., Elsner P., Maibach H.I. Characteristics of the Aging Skin. Adv Wound Care (New Rochelle) 2013; 2(1):5–10.
- Bielach-Bazyluk A., Zbroch E., Mysliwiec H., et al. Sirtuin 1 and Skin: Implications in Intrinsic and Extrinsic Aging-A Systematic Review. Cells 2021; 10(4): 813.
- Chang A.L.S., Atzmon G., Bergman A., et al. Identification of genes promoting skin youthfulness by genome-wide association study. J Invest Dermatol 2014; 134(3): 651–657.
- Xu J., Spitale R.C., Guan L., et al. Novel Gene Expression Profile of Women with Intrinsic Skin Youthfulness by Whole Transcriptome Sequencing. PLoS One 2016; 11(11): e0165913.
- Vandiver A.R., Irizarry R.A., Hansen K.D., et al. Age and sun exposure-related widespread genomic blocks of hypomethylation in nonmalignant skin. Genome Biol 2015; 16(1): 80.
- Zhang S., Duan E. Fighting against Skin Aging: The Way from Bench to Bedside. Cell Transplant 2018; 27(5): 729–738.
- Widgerow A.D., Cohen S.R., Fagien S. Preoperative Skin Conditioning: Extracellular Matrix Clearance and Skin Bed Preparation, A New Paradigm. Aesthet Surg J 20198; 39(Suppl 3): S103–S111.
- Alam M., Hughart R., Champlain A., et al. Effect of Platelet-Rich Plasma Injection for Rejuvenation of Photoaged Facial Skin: A Randomized Clinical Trial. JAMA Dermatol 2018; 154(12): 1447–1452.
- Bonferoni M.C., Caramella C., Catenacci L., et al. Biomaterials for Soft Tissue Repair and Regeneration: A Focus on Italian Research in the Field. Pharmaceutics 2021; 13(9): 1341.
- Deglesne P.A., Arroyo R., Ranneva E., et al. In vitro study of RRS HA injectable mesotherapy/biorevitalization product on human skin fibroblasts and its clinical utilization. Clin Cosmet Invest Dermatol 2016; 9: 41–53.
- Baspeyras M., Rouvrais C., Liégard L., et al. Clinical and biometrological efficacy of a hyaluronic acid-based mesotherapy product: a randomized controlled study. Arch Dermatol Res 2013; 305(8): 673–682.
- Potekaev N.N., Borzykh O.B., Karpova E.I., et al. A New Approach toward the Management of Patients with Premature Skin Aging Using the Predictor Effect. Cosmetics 2023; 10(2): 49.
 +7 (495) 032-8867
+7 (495) 032-8867

