СРАВНИТЕЛЬНАЯ ЭФФЕКТИВНОСТЬ КРЕМОВ С РАЗЛИЧНОЙ КОНЦЕНТРАЦИЕЙ МОЧЕВИНЫ КОСМЕТИЧЕСКОЙ СЕРИИ УрокрЭМ® ПРИ КСЕРОЗЕ КОЖИ
20.12.2023
Erid: 2RanymDce7z
Бутарева М.М.1, 2, Кобяцкая Е.Е.1, Мецгер А.В.1, Исраелян З.Э.1,
Петрова С.Ю.3, 4, Альбанова В.И.5, Ноздрин К.В.3
1 Федеральное государственное автономное образовательное учреждение высшего образования
Первый Московский государственный медицинский университет имени И. М. Сеченова
Министерства здравоохранения Российской Федерации, Москва
2 Клиника «Бьюти Тренд», Москва
3 АО «Ретиноиды», Москва
4 ФГБНУ «Научно-исследовательский институт вакцин и сывороток имени И.И. Мечникова»
Министерства науки и высшего образования, Москва
5 Московский областной научно-исследовательский клинический институт имени М.Ф. Владимирского, Москва
Введение
Мочевина — гигроскопический компонент рогового слоя, поддерживающий его гидратацию в составе натурального увлажняющего фактора [1]. Уже более века топические средства с мочевиной применяются для ухода за кожей в формате увлажняющего и/или кератолитического агента органического происхождения в зависимости от концентрации [2–6].
Мочевина (карбамид, диамид угольной кислоты) — органическое соединение с химической формулой CH₄N₂O, конечный продукт метаболизма белка у млекопитающих и некоторых рыб [1]. При дефиците мочевины ухудшается способность рогового слоя регулировать трансэпидермальную потерю воды (ТЭПВ), в результате развиваются симптомы сухости кожи, могут появиться гиперкератоз и зуд [1, 3].
Мочевина обладает выраженными увлажняющими свойствами, удерживая значительное количество молекул воды и повышая устойчивость рогового слоя к осмотическому стрессу [3, 7]. Однако роль мочевины этим не ограничивается. Исследования показали, что мочевина является важным регулятором функционирования живых клеток эпидермиса, в частности она влияет на пролиферацию базальных кератиноцитов и процессы ороговения [2, 7], а также на выработку антимикробных пептидов [8].
Кератиноциты экспрессируют функционально активные переносчики мочевины (UT-A1, UT-A2, аквапорин-3 и аквапорин-9). Было обнаружено, что в клетках этого типа поглощение мочевины связано с активной регуляцией транскрипционной экспрессии генов, кодирующих транспортеры мочевины. Мочевина также усиливает экспрессию генов филаггрина, лорикрина и трансглутаминазы-1 — белков, которые важны для дифференцировки кератиноцитов, а также экспрессию генов противомикробных пептидов — кателицидина и β-дефензина-2. Мочевина влияет и на синтез липидов эпидермиса. Вышеперечисленное способствует улучшению барьерной функции кожи [3, 8]. В более высоких концентрациях мочевина может денатурировать такие белки, как кератины, разрывая их водородные связи и вызывая конформационные изменения в их белковой структуре [2, 3]. Также мочевина облегчает транспорт противогрибковых и кортикостероидных препаратов через кожу и ногти [3].
Топические средства с мочевиной применяются во всем мире и зарекомендовали себя как препараты с высоким профилем безопасности. В целом они очень хорошо переносятся кожей. Иногда при использовании высоких концентраций мочевины может наблюдаться легкое раздражение кожи. Это побочное нежелательное явление носит временный характер и обычно проходит самостоятельно [9, 10].
На российском рынке представлены лечебные косметические средства с мочевиной разной концентрации, что обеспечивает большую гибкость в ее назначении. Прежде чем выбрать наиболее подходящий продукт, необходимо учитывать нозологию, степень тяжести процесса и его распространенность, а также топографическую зону нанесения препарата и возраст пациента [11, 12]. Средства с низкой концентрацией мочевины (2–10%), как правило, показаны для увлажнения и восстановления барьерной функции кожи, средней концентрации (10–30%) работают как увлажнители и кератолитики, высокой концентрации (≥ 30%) — это мощные кератолитики [9, 11–14].
Цель исследования. Сравнительная оценка клинической эффективности использования кремов, содержащих 5 и 10% мочевины, в коррекции ксероза кожи.
Материалы и методы
Участники исследования
В проспективное контролируемое клиническое исследование включены 90 пациентов (мужчины и женщины) с ксерозом кожи конечностей (кисти, предплечья, голени, стопы) в возрасте от 18 до 60 лет. Все пациенты разделены на две группы, сопоставимые по полу и по возрасту.
- 1-я группа — 45 человек (20 мужчин и 25 женщин) в возрасте от 18 до 60 лет, средний возраст 43,6 ± 3,5 года. Применение крема УрокрЭМ®5, содержащего 5% мочевины, 2 раза в день 30 дней. Контроль: применение основы крема УрокрЭМ, содержащей глицерин 10%, жидкий парафин, глицин, воду и феноксиэтанол, 2 раза в день 30 дней на одну из симметричных областей с ксерозом. Например, тыльные поверхности правой и левой кистей. На правую кисть руки наносят УрокрЭМ®5, а на левую кисть — УрокрЭМ (контроль). Если у пациента были еще какие-либо участки ксероза кожи, их обрабатывали УрокрЭМ®5.
- 2-я группа — 45 человек (18 мужчин и 27 женщин) в возрасте от 18 до 60 лет, средний возраст 45,8 ± 4,1 года. Применение крема УрокрЭМ®10, содержащего 10% мочевины, 2 раза в день 30 дней. Контроль: применение основы крема УрокрЭМ 2 раза в день 30 дней на одну из симметричных областей с ксерозом. Например, тыльные поверхности правой и левой кистей. На правую кисть руки наносят УрокрЭМ®10, а на левую кисть — УрокрЭМ (контроль). Если у пациента были еще какие-либо участки ксероза кожи, их обрабатывали УрокрЭМ®10.
Критерии включения
- Мужчины и женщины от 18 до 60 лет.
- Согласие пациента на участие в лечении.
- Подтвержденный диагноз «ксероз кожи» (L85.3).
Критерии невключения
- Аллергические реакции или индивидуальная непереносимость компонентов косметических средств в анамнезе.
- Участие в другом клиническом исследовании в период проведения данного исследования.
Критерии исключения
- пациента от участия.
- Возникновение нежелательных явлений.
Период наблюдения за пациентами — 30 дней. Количество визитов для каждого пациента — 2: в 1-й день и на 30-й день лечения.
Оцениваемые параметры
- Измерение площади ксероза кожи в 1-й и 30-й дни лечения отдельно по каждой группе в процентах согласно правилу «девяток» для взрослых: рука, половина ноги, половина спины, грудь, живот, голова — по 9%, промежность и кисть руки — 1% [15].
- Оценка зуда кожи до и после назначения косметических средств в баллах, где: 0 — отсутствие зуда; 1 — легкий зуд, возникает изредка; 2 — легкий зуд, появляется часто и самостоятельно проходит; 3 — легкий зуд, но беспокоит постоянно; 4 — зуд ощутимый, беспокоит и периодически приводит к расчесам, но не постоянный; 5 — зуд ощутимый, беспокоит и периодически приводит к расчесам, постоянный; 6 — зуд ощутимый, приводит к расчесам, постоянный, отвлекает от повседневной деятельности; 7 — интенсивный зуд, приводит к расчесам, постоянный, отвлекает от повседневной деятельности; 8 — интенсивный зуд с расчесами на коже, нарушает сон; 9 — интенсивный зуд с расчесами на коже, нарушением ночного сна и болевым компонентом; 10 — нестерпимый зуд.
- Оценку результатов увлажнения и ТЭПВ в 1-й и 30-й дни лечения проводили с помощью дерматоскопии, корнеометрии и вапометрии на аппаратах ARAMO SG с программой Skin XPPRO (Aram Huvis Co., Ltd, Южная Корея); Monaderm Combined unit CM825/SM815/CT580 (Courage + Khazaka electronic GmbH, Германия); Vapometer SWL4001 (Delfin, Финляндия).
- Оценка общих результатов коррекции сухости кожи:
- отличные (отсутствие ксероза кожи, отсутствие субъективных ощущений, по результатам корнеометрии — увлажненная кожа);
- хорошие (слабые и ограниченные проявления признаков ксероза, уменьшение площади ксероза кожи, уменьшение или отсутствие субъективных ощущений, по результатам корнеометрии — увлажненная кожа);
- удовлетворительные (уменьшение площади ксероза кожи, уменьшение субъективных ощущений, по результатам корнеометрии — сухая кожа);
- неудовлетворительные (отрицательная динамика или отсутствие улучшения, по результатам корнеометрии — сухая кожа).
Статистическая обработка данных
Результаты обрабатывали с помощью пакета прикладных статистических программ Microsoft Excel, версия 2010. Вычисляли следующие величины: среднее (µ), стандартное отклонение (σ). Для сравнения двух групп использовали критерий Стьюдента (t). Если полученные данные имели распределение с большими выбросами либо не поддавались нормальному распределению, находили медиану (Ме) и интерквартильный размах (IQR) [16].
Анализ качественных признаков: вычисление выборочной процентной доли единиц, имеющих изучаемый признак от общего числа единиц. Для оценки статистической значимости различий в группах, поскольку в некоторых из них изучаемый признак составлял более 75%, использовали метод углового преобразования Фишера с расчетом вспомогательной переменной (φ), стандартной ошибки вспомогательной переменной (Sφ) и 95% доверительного интервала (95% ДИ). Критической величиной уровня значимости считали α = 0,05 [17].
Результаты
До начала применения косметических средств у всех пациентов (как в 1-й, так и во 2-й группе) на коже, помимо умеренной сухости, присутствовали шелушение, слабые проявления растрескивания кожи и эритемы. Все пациенты, принимавшие участие в исследовании, завершили его. За период наблюдения не было зафиксировано аллергических реакций или индивидуальной непереносимости к компонентам используемых средств, участия пациентов в другом клиническом исследовании в период проведения данного исследования или отказа пациентов от участия.
Было проведено измерение площади ксероза кожи, на которую затем наносили топические средства с мочевиной, перед и на 30-й день их использования. Особые области (кожа головы, губы, веки, аногенитальная область) у пациентов не были затронуты. Результаты по каждой группе представлены в табл. 1.
Как видно из табл. 1, площадь поражения кожи у пациентов 1-й и 2-й групп была сопоставима. Статистически значимое уменьшение площади ксероза кожи выявлено при применении как крема УрокрЭМ®5; так и крема УрокрЭМ®10 (р < 0,001). Различий между группами по уменьшению площади ксероза кожи не отмечено.
Таблица 1. Площадь поражения кожи у пациентов до и после применения средств с мочевиной, %
|
Группа пациентов |
До |
На 30-й день |
t* |
р |
||
|
µ |
σ |
µ |
σ |
|||
|
1-я группа |
11,4 |
2,1 |
2,3 |
1,1 |
25,8 |
< 0,001 |
|
2-я группа |
12,5 |
3,2 |
3,1 |
1,2 |
18,5 |
< 0,001 |
Примечание. <*> — t-критерий Стьюдента при сравнении результатов в группе до и после применения средств с мочевиной при числе степеней свободы ν = 88. 1-я группа — уход за кожей с помощью УрокрЭМ®5; 2-я группа — УрокрЭМ®10.
Оценка зуда кожи до и после назначения косметических средств по 10-балльной шкале представлена на рис. 1 и в табл. 2.
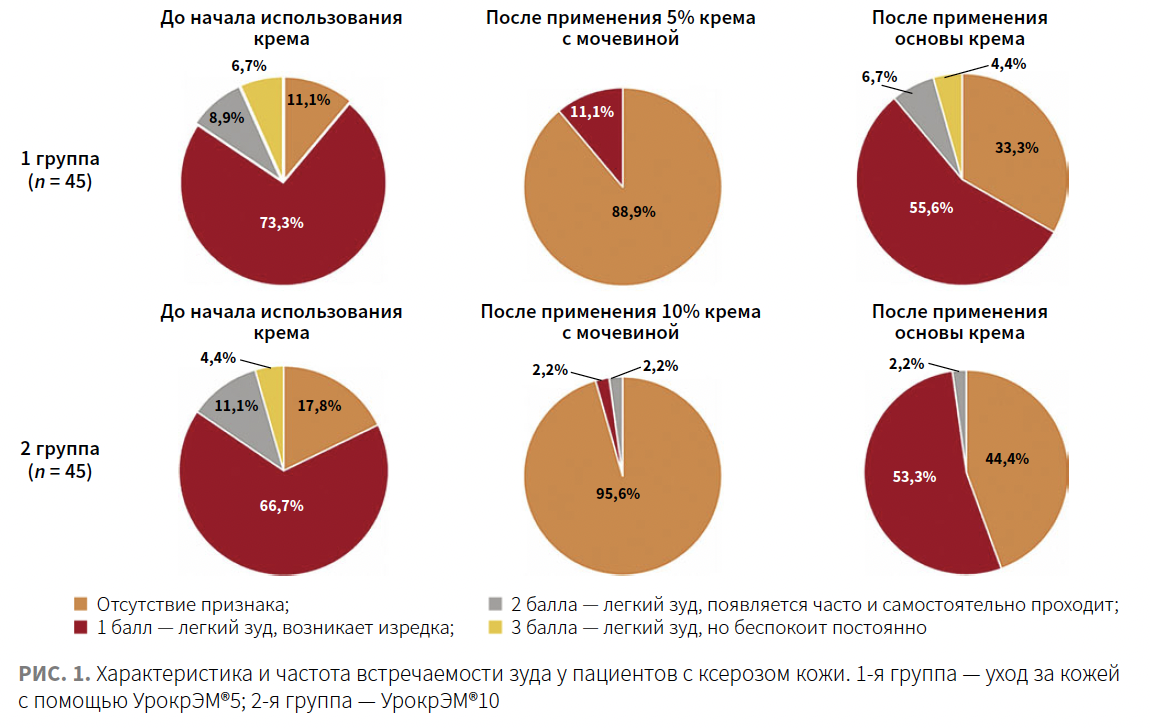
Таблица 2. Анализ частоты отсутствия зуда у пациентов до и после использования лечебной косметики с мочевиной
|
Группа пациентов |
Количество и процент пациентов без зуда, n (%) |
Вспомогательная |
95% ДИ, % |
|
1-я группа до начала ухода за кожей (n = 45) |
5 (11,1) |
0,68 |
3,5–22,1 |
|
1-я группа на 30 день ухода за кожей (n = 45) |
40 (88,9) |
2,46 |
77,9–96,5 |
|
1-я группа на 30 день ухода за кожей основой крема (n = 45) |
15 (33,3) |
1,23 |
20,1–48,0 |
|
2-я группа до начала ухода за кожей (n = 45) |
8 (17,8) |
0,87 |
7,9–30,6 |
|
2-я группа на 30 день ухода за кожей (n = 45) |
43 (95,6) |
2,72 |
87,5–99,6 |
|
2-я группа на 30 день ухода за кожей основой крема (n = 45) |
20 (44,4) |
1,46 |
29,9–59,4 |
Примечание. t = 2,015 при числе степеней свободы ν = 44 [31]. 1-я группа — уход за кожей с помощью УрокрЭМ®5; 2-я группа — УрокрЭМ®10.
До начала использования увлажняющих кремов большая часть пациентов как в 1-й (УрокрЭМ®5), так и во 2-й группе (УрокрЭМ®10) жаловались на легкий, возникающий изредка кожный зуд (1 балл). Ощутимого, интенсивного и нестерпимого зуда у пациентов не было. После применения кремов с мочевиной у большинства пациентов зуд отсутствует — у 40 человек (88,9%) в 1-й группе и у 43 человек (95,6%) во 2-й группе. Причем разница между 1-м и 30-м днем статистически значима как в 1-й, так и во 2-й группе (р < 0,05).
Следует отметить снижение зуда и там, где применяли основу крема, но оно статистически значимо (более чем в 2 раза) меньше, чем на участках кожи, где применяли средства с мочевиной (р < 0,05), и не имеет статистически значимых различий с частотой отсутствия зуда у больных перед началом ухода за кожей (р > 0,05). Полученные данные характерны и для 1-й, и для 2-й группы.
Оценка результатов увлажнения и барьерной функции кожи в 1-й и 30-й дни лечения представлена в табл. 3. Результаты корнеометрии демонстрируют повышение увлажненности кожи у пациентов, использующих кремы с 5 и 10% мочевиной; результаты вапометрии — снижение степени ТЭПВ и в 1-й, и во 2-й группе.
Таблица 3. Объективная оценка увлажнения и барьерной функции кожи
| Метод измерения |
1-я группа (n = 45), медиана (IQR) | 2-я группа (n = 45), медиана (IQR) | ||||
|
До |
На 30-й день |
На 30-й день (основа крема) |
До |
На 30-й день |
На 30-й день (основа крема) |
|
|
Корнеометрия, |
20,05 (5,83) |
28,95 (3,13) |
25,4 (4,79) |
19,8 (4,87) |
27,45 (3,34) |
22,6 (4,75) |
|
Вапометрия, |
34,55 (3,95) |
22,95 (4,65) |
31,95 (3,73) |
33,4 (4,58) |
23,68 (3,87) |
26,89 (5,12) |
Примечание. 1-я группа — уход за кожей с помощью УрокрЭМ®5; 2-я группа — УрокрЭМ®10.
Оценка общих результатов коррекции сухости кожи представлена в табл. 4. По результатам лечения у 40 пациентов (88,8%) в 1-й группе и у 38 пациентов (84,4%) во 2-й группе клинический эффект можно оценить как отличный, что было подтверждено аппаратными методами диагностики. Неудовлетворительные результаты отсутствовали. Следует отметить положительные результаты и на тех поверхностях кожи пациентов, где применяли основу крема, в которую входит глицерин. Однако эти результаты существенно ниже.
Таблица 4. Результаты лечения
|
Группа пациентов |
Отличные, |
Хорошие, |
Удовлетворительные, |
Неудовлетворительные, |
|
1-я группа (n = 45) |
||||
|
На 30-й день применения |
40 (88,9) |
5 (11,1) |
0 |
0 |
|
На 30-й деньприменения основы крема |
35 (55,6) |
10 (22,2) |
10 (22,2) |
0 |
|
2-я группа (n = 45) |
||||
|
На 30-й день применения |
38 (84,4) |
5 (11,1) |
2 (4,4) |
0 |
|
На 30-й деньприменения основы крема |
21 (46,7) |
15 (33,3) |
9 (20) |
0 |
Примечание. 1-я группа — уход за кожей с помощью УрокрЭМ®5; 2-я группа — УрокрЭМ®10.
Присутствие неприятных ощущений у пациентов при использовании косметических средств по группам: зуд, жжение, боль, другое представлено в табл. 5.
Таблица 5. Присутствие неприятных ощущений у пациентов при использовании косметических средств
| Субъективное ощущение |
1-я группа (n = 45) |
2-я группа (n = 45) |
||
|
n |
% |
n |
% |
|
|
Зуд |
0 |
0 |
0 |
0 |
|
Жжение |
3 |
6,7 |
2 |
4,4 |
|
Ощущение липкости после применения |
8 |
17,8 |
5 |
11,1 |
Примечание. 1-я группа — уход за кожей с помощью УрокрЭМ®5; 2-я группа — УрокрЭМ®10.
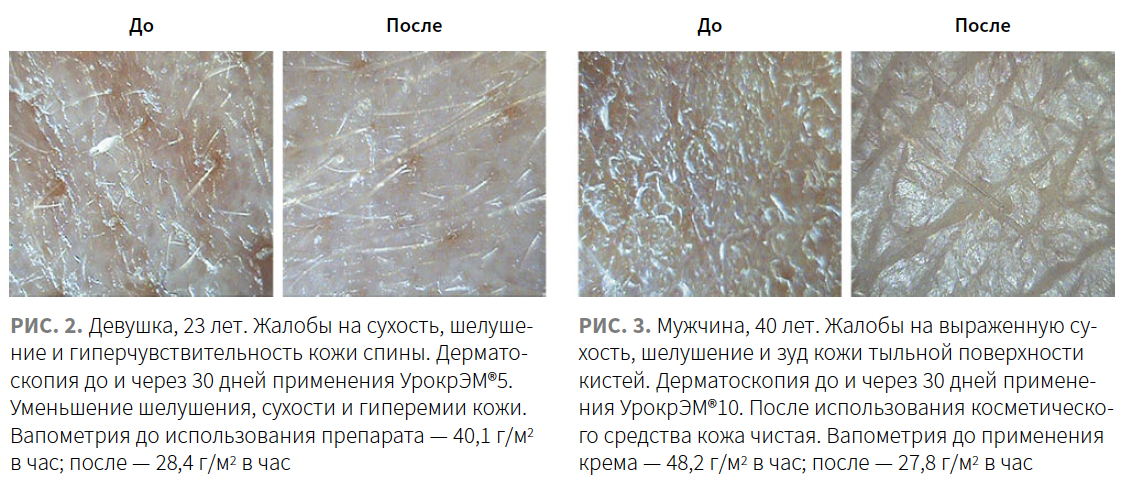
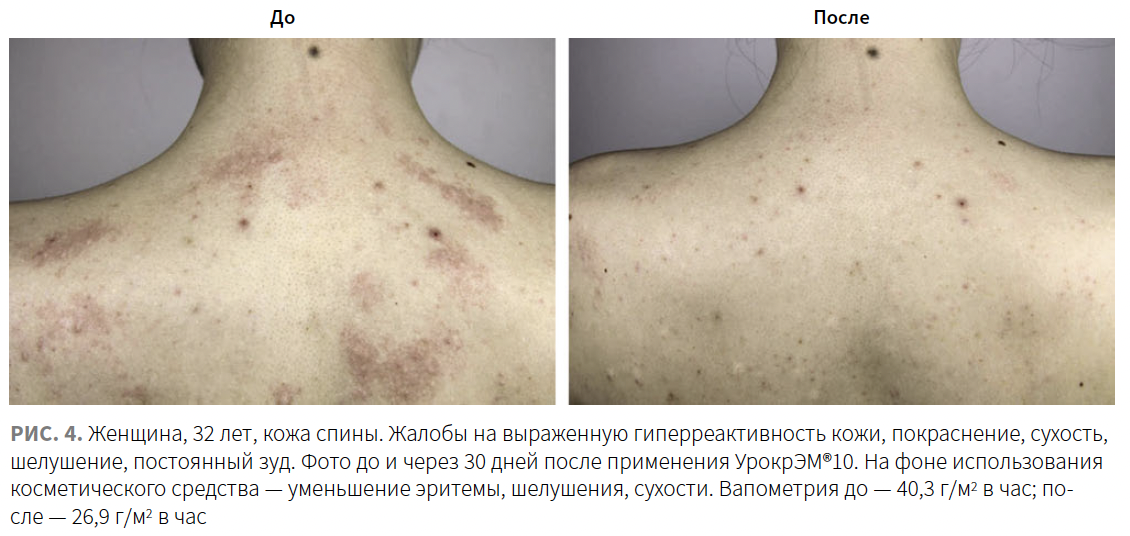
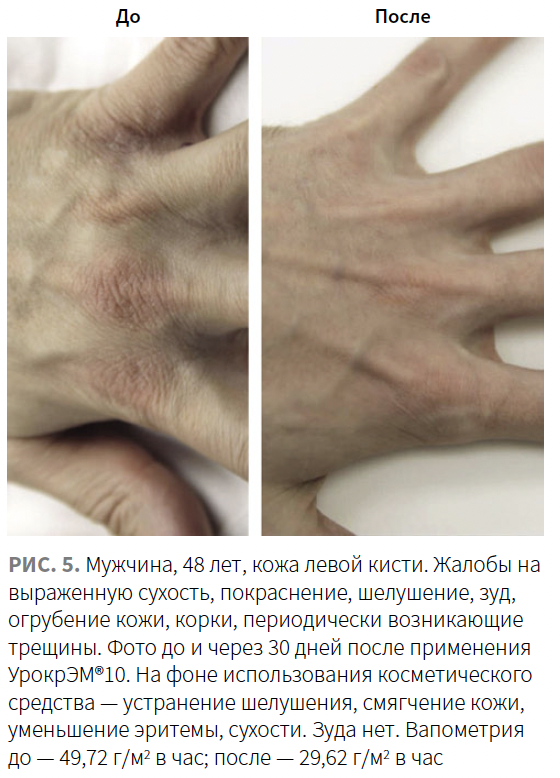
В целом применение лечебной косметики с мочевиной не вызывало у пациентов выраженных неприятных ощущений. Зуда или усиления уже имеющегося зуда при нанесении крема не испытывал ни один пациент. В 1-й группе 3 человека (6,7%) жаловались на небольшое чувство жжения после применения крема; во 2-й группе — 2 человека (4,4%). 8 пациентов в 1-й группе (17,8%) и 5 пациентов во 2-й группе (11,1%) обращали внимание на ощущение липкости кожи после нанесения средств. За период наблюдения осложнений после применения средств зафиксировано не было. Клинические примеры представлены на рис. 2–5.
Обсуждение
Как видно из результатов исследования, у всех пациентов можно отметить хорошую переносимость представленных наружных средств и положительный клинический эффект разной степени выраженности.
Так, использование препаратов позволило значительно уменьшить площадь распространенности ксероза — с 11,4 до 2,3% (на 9,1%) в 1-й группе и с 12,5 до 3,1% (на 9,4%) во 2-й группе. Следует отметить, что сухие участки кожи сохранились в основном только на местах, где применяли основу крема. Об этом же свидетельствует и редко отмечаемый пациентами зуд на участках, обрабатываемых в течение 1 мес УрокрЭМ®5 иУрокрЭМ®10. Следует выделить, что все больные как в 1-й, так и во 2-й группе заметили уменьшение не только интенсивности, но и кратности эпизодов зуда в течение дня. Применение основы крема УрокрЭМ принесло лишь незначительное его облегчение.
В целом применение у пациентов кремов с мочевиной разной концентрации по всем параметрам показало схожие результаты. Более чем у 80% пациентов в обеих группах отмечены отличные результаты лечения. Ни у одного пациента не выявлено отрицательной динамики течения ксероза кожи или отсутствия улучшения состояния. Аппаратные методы диагностики еще раз подтверждают усиление увлажненности кожи у пациентов после применения данных средств лечебной косметики, а также, что наиболее существенно, — уменьшение ТЭПВ. Данный факт может являться косвенным подтверждением усиления барьерной функции эпидермиса под действием мочевины, что согласуется с данными литературы [12, 14].
Мы не стали бы делать поспешных выводов о том, что разные концентрации мочевины (5 и 10%) оказывают одинаковое действие на кожу. Первоначально исследуемые группы пациентов характеризовались умеренными проявлениями ксероза. Возможно, что при применении данных средств у пациентов с более выраженными признаками сухости мы смогли бы увидеть и разницу в увлажняющих эффектах между разными концентрациями действующего вещества.
Существенной динамики кожного процесса в сторону снижения признаков ксероза — как по объективным, так и по субъективным параметрам — на участках, где применяли основу крема, не отмечено. Результаты значительно ниже, чем при применении крема того же состава, но с мочевиной. Надо признать, мы ожидали большего от основы крема, поскольку туда входит глицерин 10%, который не только является хорошим увлажняющим агентом, но и обладает массой дополнительных полезных свойств [15].
Заключение
Препараты, содержащие мочевину в концентрации до 10%, давно зарекомендовали себя как средства с прекрасными увлажняющими и восстанавливающими свойствами, которые помогают достаточно быстро устранить сухость, шелушение, зуд и эритему при ксерозе коже. Кремы с 5% и 10% мочевиной позволяют обеспечить оптимальный базовый уход за кожей, склонной к ксерозу или уже имеющей его признаки.
Литература
- Friedman A.J., von Grote E.C., Meckfessel M.H. Urea: a clinically oriented overview from bench to bedside. J Drugs Dermatol 2016; 15(5): 633–639.
- Pan M., Heinecke G., Bernardo S., et al. Urea: a comprehensive review of the clinical literature. Dermatol Online J 2013; 19(11): 20392.
- Celleno L. Topical urea in skincare: a review. Dermatol Ther 2018; 31(6): e12690.
- Berardesca E., Cameli N. Non-invasive assessment of urea efficacy: a review. Int J Clin Pract 2020; 74(Suppl 187): e13603.
- Ихтиоз: клинические рекомендации. Общероссийская общественная организация «Российское общество дерматовенерологов и косметологов». 2020. https://cnikvi.ru/docs/clinic_recs/klinicheskie-rekomendatsii-2019-2020/files/Ихтиоз%2008.10.2020.docx
- Paller A.S., Butala S., Hand J.L., Corona R. Inherited ichthyosis: Overview of management. Nov 15, 2023. https://www.uptodate.com/contents/inherited-ichthyosis-overview-of-management
- Trullàs-Cabanes C., Mirada-Ferré A., Salomon-Niera M. El valor de la urea en el cuidado y tratamiento de la piel. Revista Dermatológica Perú 2008; 18(1): 41–44.
- Grether-Beck S., Felsner I., Brenden H., et al. Urea uptake enhances barrier function and antimicrobial defense in humans by regulating epidermal gene expression. J Invest Dermatol 2012; 132(6): 1561–1572.
- Starace M., Alessandrini A., Piraccini B.M. Clinical evidences of urea at high concentration on skin and annexes. Int J Clin Pract 2020; 74(Suppl 187): e13740.
- Piraccini B.M., Alessandrini A., Bruni F., Starace M. Acute periungueal dermatitis induced by application of urea-containing cream under occlusion. J Dermatol Case Rep 2012; 6(1): 18–20.
- Sethi A., Kaur T., Malhotra S.K., Gambhir M.L. Moisturizers: the slippery road. Indian J Dermatol 2016; 61(3): 279–287.
- Альбанова В.И., Калинина О.В., Петрова С.Ю. Применение мочевины для коррекции нарушений кожного барьера. Вестник дерматологии и венерологии 2022; 98(4): 67–75.
- Dall’Oglio F., Tedeschi A., Verzì A.E., et al. Clinical evidences of urea at medium concentration. Int J Clin Pract 2020; 74 Suppl 187: e13815.
- Piquero-Casals J., Morgado-Carrasco D., Granger C., et al. Urea in dermatology: a review of its emollient, moisturizing, keratolytic, skin barrier enhancing and antimicrobial properties. Dermatol Ther (Heidelb) 2021; 11(6): 1905–1915.
- Augustin M., Wilsmann-Theis D., Körber A., et al. Diagnosis and treatment of xerosis cutis — a position paper. J Dtsch Dermatol Ges 2019; 17(Suppl 7): 3–33.
- Гланц С. Медико-биологическая статистика. М.: Практика, 1999.
- Гржибовский А.М. Доверительные интервалы для частот и долей. Экология человека 2008; 5: 57–60.
Реклама. ООО «Ретиноиды»

