РОССИЙСКИЙ КОНСЕНСУС ЭКСПЕРТОВ ПО ПРИМЕНЕНИЮ ИМПЛАНТАТА СКУЛЬПТРА™ (ПОЛИ-L-МОЛОЧНАЯ КИСЛОТА) В ЭСТЕТИЧЕСКОЙ МЕДИЦИНЕ
22.07.2020
Участники Экспертного совета: Гавашели Л.Г. (Москва), Дмитриева И.П. (Санкт-Петербург), Дьяченко Ю.Ю. (Москва), Захаров Д.Ю. (Екатеринбург), Колиева М.Х. (Москва), Красносельских М.А. (Санкт-Петербург), Макарова О.Б. (Москва), Чернышева М.П. (Москва)
Под редакцией Дмитриевой И.П. (Санкт-Петербург)
Материалы, представленные в Российском консенсусе, основаны на клиническом опыте 8 экспертов, которые провели тысячи инъекций имплантата Скульптра™. В нем также учтены рекомендации зарубежных коллег и последние тенденции в области эстетической медицины.
Надеемся, что эти рекомендации будут полезны врачам эстетической медицины с точки зрения достижения убедительных результатов и повышения безопасности косметологической коррекции с применением Скульптра™.
Историческая справка
Применение в косметологии современных биостимулирующих препаратов на основе поли-L-молочной кислоты (poly-L-lactic acid, PLLA) началось в 1990-е гг . Первый продукт, содержащий частицы PLLA, был зарегистрирован в ЕС в 1999 г. под названием New-Fill®. Его рекомендовали для коррекции липоатрофии лица у ВИЧ-инфицированных пациентов, получающих антиретровирусную терапию. В период с 1999 по 2004 гг. процедуры с использованием имплантата New-Fill® были проведены более чем 150 000 пациентам с липоатрофией лица [1].
В 2004 г. продукт получил новое название — Sculptra® и начал активно применяться в эстетической медицине у здоровых пациентов, имеющих различные проявления процесса структурного старения лица.
В 2004 г. FDA (Управление по надзору за качеством пищевых продуктов и медикаментов США) одобрило применение Sculptra® для восстановления объема мягких тканей лица при липоатрофии у ВИЧ-инфицированных пациентов. Позднее, в 2009 г., показания к применению имплантата были изменены: рекомендовано его использование у людей с нормальным иммунологическим статусом для коррекции глубоких носогубных складок и других морщин лица [2].
В 2014 г. компания Galderma приобрела права на имплантат Sculptra®, включая его реализацию во всем мире, кроме стран Западной Европы, где дистрибьютором продукта является компания Sinclair Pharma (Великобритания).
В РФ медицинское изделие Sculptra® (СкульптраТМ) было зарегистрировано группой компаний Санофи в 2009 г., а в дальнейшем перерегистрировано на компанию Gаldermа/Кью-Мед АБ, Швеция (регистрационное удостоверение выдано Росздравнадзором 03.04.2017 г., номер регистрационного удостоверения: ФСЗ 2009/05553) [3]. Sculptra® производится в Италии на заводе компании Sanofi по контракту с компанией Кью-Мед АБ для всех стран мира, включая РФ.
Процесс структурного старения лица
Процесс старения лица — мультифакторный, на него влияет множество причин, как внутренних, так и внешних.
С возрастом кожа лица изменяется — снижаются ее тургор и эластичность, появляются мелкие морщины. Причиной этого является прогрессивное снижение содержания основных структурных элементов внеклеточного матрикса (коллагена, эластина, гликозаминогликанов) и изменение их характеристик. Истончается средний слой кожи (собственно дерма), снижается способность кожи удерживать влагу (рис. 1) [4–8].

Структурные изменения затрагивают не только кожу, но и все подлежащие слои: подкожно-жировую клетчатку (ПЖК), связки, поверхностные и глубокие жировые пакеты, мышечную, хрящевую и костную ткани. Инволюционные изменения любого из этих слоев влияют на другие и на общий вид лица. Прогрессивная потеря объема жировых пакетов, их смещение, ослабление связок, резорбция хрящевых и костных структур, гипертонус мышц-депрессоров приводят к появлению на лице складок, борозд, зон депрессии, птозу мягких тканей, изменению контуров лица и шеи [5–8].
Первые признаки старения появляются уже в возрасте 30 лет и усугубляются с течением времени, особенно под воздействием внешних факторов: избыточной инсоляции, курения, погрешностей питания и т.д. [9].
В последние десятилетия в эстетической медицине произошла настоящая революция, связанная с появлением новых инъекционных продуктов, развитием аппаратных, клеточных и нитевых методик. Каждый год появляются новые и совершенствуются существующие методы лечения. Статистика последних лет показывает, что малоинвазивные нехирургические вмешательства становятся все более популярными во всех странах, их количество существенно превышает количество хирургических операций. Американское общество эстетической пластической хирургии (ASAPS) опубликовало данные, согласно которым в 2019 г. в США было проведено примерно 1,5 млн хирургических процедур и более 2,5 млн инъекционных эстетических процедур. Общая стоимость инъекционных эстетических процедур в 2019 г. составила более 1,6 млрд долларов, при этом их число выросло на 17,8% по сравнению с 2015 г. [10].
Современная стратегия косметической коррекции признаков структурного старения лица подразумевает использование комбинации различных методов воздействия на разные анатомические структуры и ткани, что позволяет достигать наглядных и стойких результатов. Параллельно активно разрабатываются и внедряются различные методики эстетической коррекции тела. При этом рекомендуется максимально индивидуализировать протоколы коррекции, учитывая возраст пациента, тип старения, особенности образа жизни и другие факторы.
Несмотря на полиэтиологичность, процесс внешнего старения имеет фундаментальный механизм, связанный с изменениями гомеостаза коллагена — основного структурного компонента кожи [11, 12].
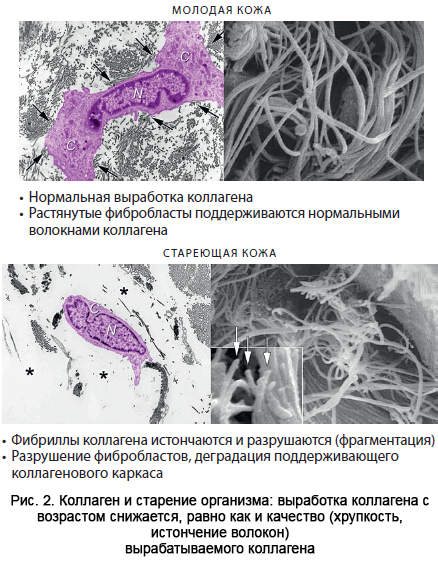
Коллаген — фибриллярный белок, составляющий основу соединительной ткани организма (сухожилия, кость, хрящ, дерма и т.п.), обеспечивающий ее прочность и эластичность. Коллаген в организме человека продуцируется клетками соединительной ткани — фибробластами. Первый этап, внутриклеточный, включает синтез линейных молекул, их последующую модификацию и сборку тройных спиралей проколлагена, который секретируется во внеклеточную среду. Во внеклеточном матриксе происходит созревание коллагена (в дерме он представлен в основном коллагеном I и III типа): стабилизация структуры белка с последующим формированием коллагеновых фибрилл (волокон), необходимых для создания поддерживающего каркаса в коже [13, 14].
По мере старения содержание коллагена в коже снижается, при этом происходит и процесс «старения» самого белка, что приводит к повреждению его структуры и ухудшению биомеханических свойств. Возрастная деградация коллагена обусловлена рядом факторов: снижением пула активных фибробластов, повышением активности матриксных металлопротеиназ. Что в целом приводит к выраженной деградации внеклеточного матрикса дермы (рис. 2) [15]. Клинически это отражается на упругости и эластичности кожи, сопровождается формированием мелких и крупных морщин [14].
Для восстановления гомеостаза коллагена в дерме необходимо повысить синтетическую активность фибробластов. Этого можно достичь различными способами. Частички поли-L-молочной кислоты в составе Sculptrа® являются мощнейшим стимулятором неоколлагеногенеза в коже [16].
Химический состав и структура Sculptra®
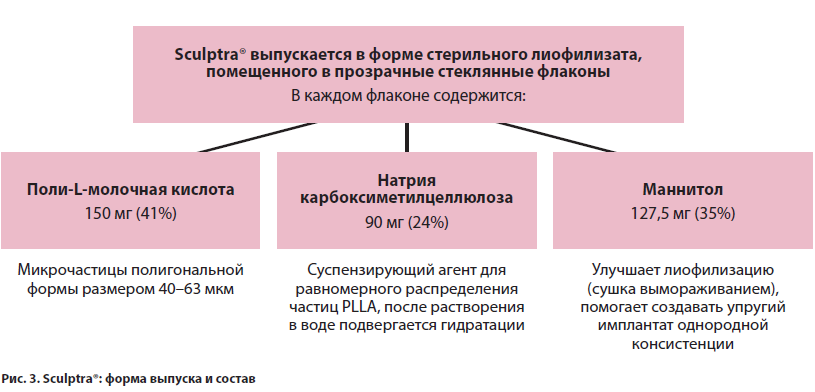
Sculptrа® поставляется в РФ в форме стерильного лиофилизата, помещенного в прозрачный стеклянный флакон. В каждом флаконе содержатся поли-L-молочная кислота 150 мг (41%), натрия карбоксиметилцеллюлоза 90 мг (24%) и маннитол 127,5 мг (35%) (рис. 3) [17].
Поли-L-молочная кислота является биоразлагаемым, биосовместимым синтетическим полимером, состоящим из мономеров L-молочной кислоты (левовращающий оптический изомер). PLLA давно и успешно используется в медицинской и фармацевтической промышленности для производства ортопедических фиксирующих устройств (штифты, стержни и болты, пластины и винты для пластической хирургии), имплантатов (внутрикостных и для мягких тканей), шовных материалов, мезонитей, катетеров, трансдермальных систем (накожные пластыри и др.), систем с контролируемым (замедленным) высвобождением активных компонентов [18–20].
PLLA представляет собой гидрофобный полимер, нерастворимый в воде. При этом другие компоненты Sculptra® — карбоксиметилцеллюлоза и маннитол — гидрофильны и растворимы в воде. В тканях с течением времени PLLA в ходе неферментативного гидролиза (с участием молекул воды) распадается на мономеры молочной кислоты, которые, в свою очередь, метаболизируются до углекислого газа (CO2) и воды [21].
Sculptra® — это биостимулятор
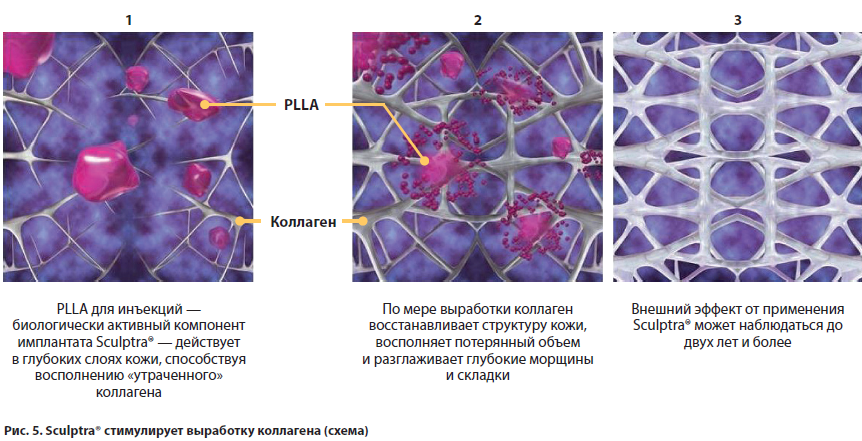
Sculptra® — это имплантат-биостимулятор, который состоит из частиц PLLA полигональной формы размером 40–63 мкм [22]. Поли-L-молочная кислота, являясь биологически активным компонентом Sculptrа®, действует в глубоких слоях кожи, обеспечивая утолщение мягких тканей путем стимуляции синтеза коллагена. По мере своей выработки коллаген восстанавливает структуру кожи, восполняет потерянный объем и разглаживает глубокие морщины и складки [20, 23, 24].
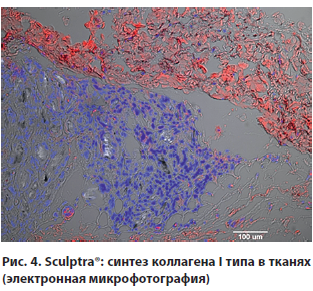
Внешний эффект от применения Sculptrа® может наблюдаться до двух и более лет [19], при этом Sculptra® «работает», стимулируя синтез коллагена I и III типа (рис. 4, 5). И это продолжительный процесс [25].
Эстетический результат не формируется мгновенно, хотя изменения в биопсийных образцах видны уже в течение 2 нед после проведения процедуры [16, 26].
Формирование нового коллагена приводит к утолщению кожи. Исследование, проведенное Mest D.R. и соавт. в 2006 г., продемонстрировало увеличение толщины кожи на 65,1% по сравнению с исходным уровнем, причем эффект сохранялся не менее 12 мес [27].
Наблюдаемые положительные эффекты сопровождаются контролируемой реакцией тканей на введение имплантата. В клиническом исследовании, проведенном Goldberg D. и соавт. в 2013 г., была обнаружена статистически значимая стимуляция синтеза коллагена I типа после инъекции PLLA на фоне отсутствующего или слабого воспалительного ответа [16]. Исследования на животных показали похожие результаты:
- 1-я неделя: незначительная воспалительная реакция в окружающих тканях на введение частиц PLLA;
- через 2 нед: выраженная активность фибробластов и их пролиферация (необходимое действие имплантата);
- через 4 нед: постепенное формирование зрелых волокон коллагена I типа [24, 28].
Sculptra®: данные клинических исследований
У имплантата Sculptra® — серьезная доказательная база по эффективности и безопасности с 20-летним опытом клинического применения в мире: с 1999 г. под названием New-Fill®, с 2004 г. — Sculptra® (рис. 6) [1].

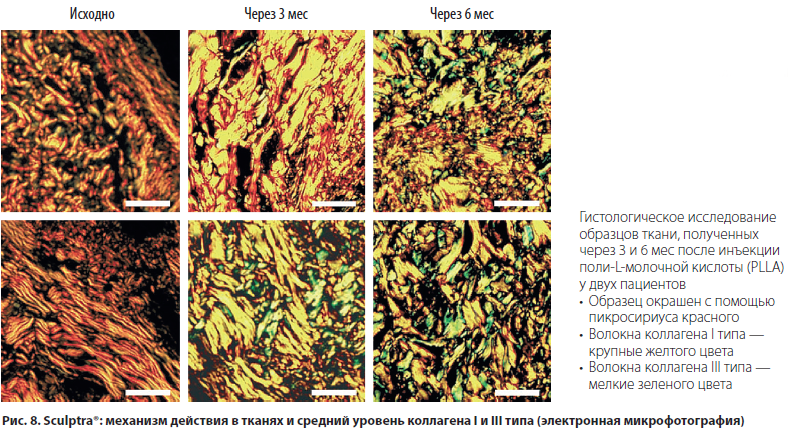
Исследование Goldberg D. и соавт. в 2013 г. биопсийного материала кожи заушной области после введения Sculptra® показывает, что частицы PLLA в тканях человека стимулируют синтез коллагена I и III типа (рис. 7, 8) [16].
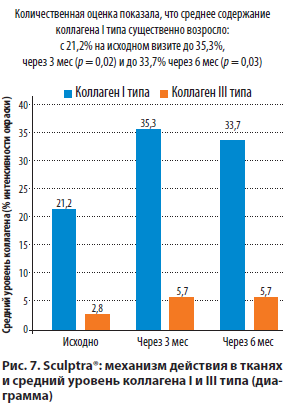
Исследование Vleggaar D. и соавт. в 2004 г. биопсийного материала кожи носогубных складок показывает, что частицы PLLA в тканях человека стимулируют синтез коллагена I и III типа и постепенно разрушаются, причем частицы PLLA не обнаруживаются через 30 мес (рис. 9) [20].
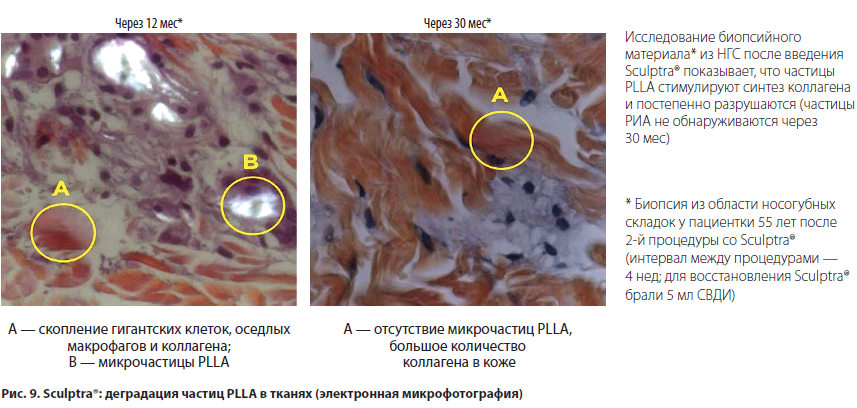
Клинические исследования New-Fill®/Sculptra®
Первым показанием для применения имплантата на основе PLLA в 1999 г. была коррекция признаков липоатрофии (уменьшение/потеря жировой ткани лица) у пациентов с ВИЧ-инфекцией, получающих антиретровирусную терапию [29, 30].
В процессе регистрации New-Fill® по этому показанию были проведены два базовых клинических исследования для оценки эффективности и безопасности имплантата (исследование VEGA и исследование Chelseа and Westminster). Позже два дополнительных исследования (Apex 002 и Blue Pаcific) были проведены для уточнения данных по безопасности продукта [30, 31].
Данные исследования проводились в том числе и для того, чтобы определить достаточное количество растворителя (стерильной воды для инъекций — СВДИ), необходимой для восстановления лиофилизата. В первых исследованиях, где для разведения использовали 3 мл СВДИ, было выявлено много побочных эффектов в виде папул и узелков, а также единичные случаи гранулем. В исследованиях Apex 002 и Blue Pаcific использовали разведение в 5 мл, что позволило значительно снизить количество побочных эффектов [1, 32].
Для изучения клинической эффективности и безопасности коррекции носогубных складок с использованием инъекционной формы PLLA (Sculptra®) в сравнении с продуктом на основе человеческого коллагена (CosmoPlast®) Narins R. и соавт. в 2010 г. провели рандомизированное исследование с участием 233 пациентов. Данное исследование показало, что видимые результаты коррекции при применении Sculptra® сохраняются на протяжении 25 мес с высоким уровнем удовлетворенности пациентов. Инъекционная форма коллагена (CosmoPlast®) обеспечивала эстетический результат на протяжении менее 3 мес (рис. 10) [19].
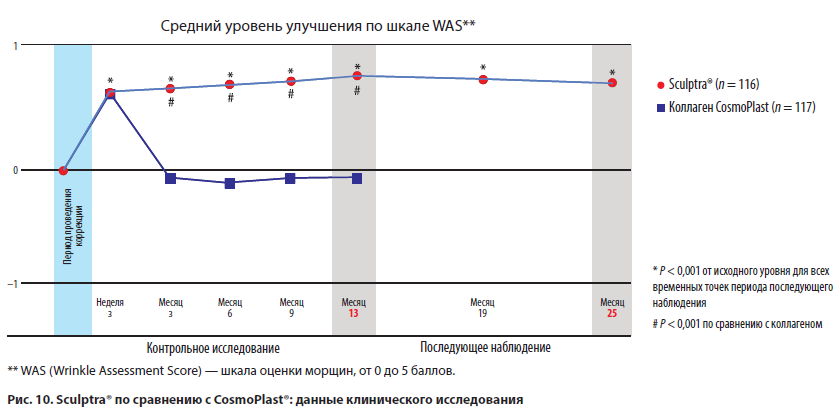
Для эффективного действия инъекций Sculptra® важно, чтобы продукт готовился, применялся и хранился с соблюдением всех рекомендаций производителя, а также экспертных рекомендаций, что позволяет минимизировать развитие возможных нежелательных реакций.
Российский консенсус по применению медицинского изделия Скульптра™
В феврале 2018 г. в г. Москве состоялось заседание Совета экспертов в области эстетической медицины по обновлению актуальной информации по препарату Скульптра™ и достижению согласия (консенсуса) по наиболее важным вопросам эстетической коррекции лица с помощью PLLA. В ходе заседания были обсуждены научные и клинические данные, мировой и личный опыт применения Sculptra®, а также рекомендации Американского и Европейского консенсусов экспертов [33, 34].
В рамках заседания экспертного Совета были разработаны рекомендации по применению препарата Скульптра™ для российских врачей (консенсус). За два года, прошедшие со времени проведения первого заседания Российского совета экспертов, рекомендации по применению Скульптра™ были внедрены в практическую медицину и претерпели ряд уточнений и усовершенствований.
Ниже приведены рекомендации Российского консенсуса по применению Скульптра™ 2018 г. с модификациями от июля 2019 г. и апреля 2020 г.
Область лица
Показания и противопоказания к применению
Перед проведением процедуры эстетической коррекции с помощью имплантата Скульптра™ необходимо тщательно собрать анамнез и выявить наличие абсолютных и относительных противопоказаний (таких, как острые или хронические кожные заболевания, признаки инфекции или воспаления в области введения или вблизи нее). Биостимулятор Скульптра™ не должен применяться у пациентов с аллергией к каким-либо его компонентам.
Поскольку безопасность применения имплантата Скульптра™ у пациентов с повышенной склонностью к образованию келоидных и гипертрофических рубцов не установлена, его не следует применять у пациентов с патологическими рубцами в анамнезе или с предрасположенностью к их формированию. Безопасность имплантата Скульптра™ для использования во время беременности, у кормящих грудью или у пациентов младше 18 лет не изучалась. Исследования взаимодействия имплантата Скульптра™ с лекарственными препаратами, другими веществами или имплантатами не проводились [17].
Профиль пациента для эстетической коррекции лица с помощью Скульптра™:
- Возраст старше 30 лет (в ряде случаев допустимо использование имплантата с 18 лет)
- Любой морфотип старения
- Сниженная эластичность тканей, дряблость кожи
- Истончение кожи и подкожных тканей
- Потеря объема лица
- Липоатрофия
- Птоз тканей
- Асимметрия лица
- Атрофические рубцы после акне
- Значительная потеря веса или планируемое похудение.
Приготовление и проведение процедуры
Расходные материалы и действия при проведении процедуры введения имплантата Скульптра™ в области лица
Этап I. ПОДГОТОВКА ИМПЛАНТАТА
- Флакон медицинского изделия Скульптра™: проверить целостность флакона, срок годности и серию, не использовать имплантат, если на флаконе есть следы нарушения герметичности, повреждения флакона, колпачка или пробки
- Стерильная вода для инъекции (СВДИ)
- Стерильные шприцы объемом 10 мл, иглы 18G
- Антисептик и стерильные салфетки для обработки флакона
Этап II. ГИДРАТАЦИЯ/ВОССТАНОВЛЕНИЕ
- Удалить защитный колпачок с флакона препарата Скульптра™
- Протереть пробку антисептиком
- Набрать 8 мл СВДИ в шприц объемом 10 мл
- Ввести СВДИ во флакон медленно (по внутренней стенке) с помощью иглы 18G через резиновую пробку, стараясь не разбивать лиофилизат на крупные фрагменты и не вспенивать суспензию
Этап III. ПРОЦЕДУРА
- Флакон с суспензией Скульптра™, восстановленной с помощью СВДИ
- Антисептик и стерильные салфетки для обработки кожи пациента в области введения имплантата
- Иглы 18G для набора суспензии из флакона
- Шприцы объемом 1–3 мл для проведения инъекций
- Стерильные иглы 26–27G длиной 13–25 мм, канюли 22–23G длиной 38–70 мм для проведения инъекций
Одним из основополагающих моментов безопасного применения медицинского изделия Скульптра™ является восстановление лиофилизата стерильной водой для инъекций. Рекомендации по необходимому для разведения объему СВДИ со временем менялись. Так, в 1999 г. рекомендованным к восстановлению New-Fill® был объем СВДИ 3 мл, в дальнейшем на основании данных клинических исследований и опыта практического применения продукта объем СВДИ был увеличен до 5 мл.
В настоящее время по данным Американского и Европейского консенсусов экспертов рекомендуется использовать 7–8 мл СВДИ для восстановления Sculptra® [33, 34].
По данным Российского консенсуса экспертов, есть преимущества в восстановлении лиофилизата Скульптра™ в одном флаконе 8 мл СВДИ.
Восстановление суспензии Скульптра™
Российские эксперты рекомендуют следующий способ восстановления суспензии Скульптра™. Восстанавливать лиофилизат необходимо при комнатной температуре минимум за 2 ч до проведения процедуры (есть рекомендации — за 24–48 ч) [33], чтобы была обеспечена необходимая гидратация материала. Не встряхивать флакон во время периода гидратации. Когда имплантат готов к инъекции, его осторожно встряхивают непосредственно перед использованием до получения однородной суспензии. Перед использованием протирают антисептиком резиновую пробку флакона, затем, используя стерильную иглу 18G, забирают необходимое количество суспензии в одноразовый стерильный шприц [17].
Далее во флакон можно добавить 1–2 мл 2% раствора лидокаина, покачивающими движениями аккуратно смешать раствор лидокаина с суспензией. Таким образом должно получиться 9–10 мл гомогенной суспензии, жидкая фаза которой представлена 8 мл СВДИ и 1–2 мл 2% раствора лидокаина.
Не рекомендуется долго хранить набранную суспензию в шприце, так как происходит оседание частиц. Восстановленный продукт можно хранить не более 72 ч при комнатной температуре (не более 30 °C) или в холодильнике (2–8 °C). Повторное использование приготовленной суспензии недопустимо [17].
Обсуждается и другой способ восстановления лиофилизата Скульптра™. Baumann K. и соавт. в 2020 г. показали, что физико-химические характеристики суспензии PLLA сразу после добавления СВДИ и интенсивного встряхивания сравнимы с таковыми, полученными путем более длительной гидратации продукта. Исследователи восстанавливали лиофилизат Скульптра™ непосредственно перед инъекцией, последовательно добавляя СВДИ (5 мл, затем 3 мл) и тщательно перемешивая. В настоящее время проводятся клинические исcледования для подтверждения данных лабораторных испытаний (рис. 11). Эти исследования важны для клинической практики, так как часто возникает необходимость в готовом продукте непосредственно перед процедурой [35].
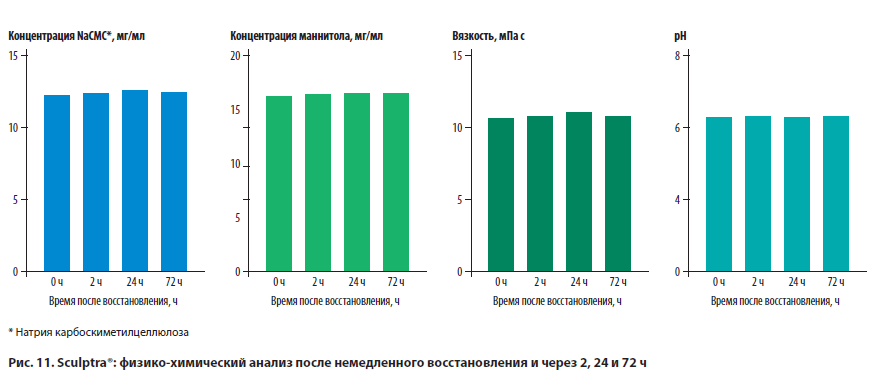
В действующей Российской инструкции по применению Скульптра™ не указано о возможности добавления анестезирующего средства: данная рекомендация основывается на практическом опыте экспертов и рекомендациях консенсусов Европейских и Американских экспертов [33, 34].
Техники введения
Имплантат Скульптра™ вводится субдермально, в подкожную жировую клетчатку, так как при поверхностных инъекциях существует риск возникновения узелков в месте инъекций, что свидетельствует о неправильной технике введения или об избыточном количестве введенной суспензии. В некоторых областях (височная зона) рекомендовано вводить продукт под SMAS, поверхностный листок темпоропариетальной фасции, учитывая очень тонкий слой подкожной жировой клетчатки в этой зоне (рис. 12А).
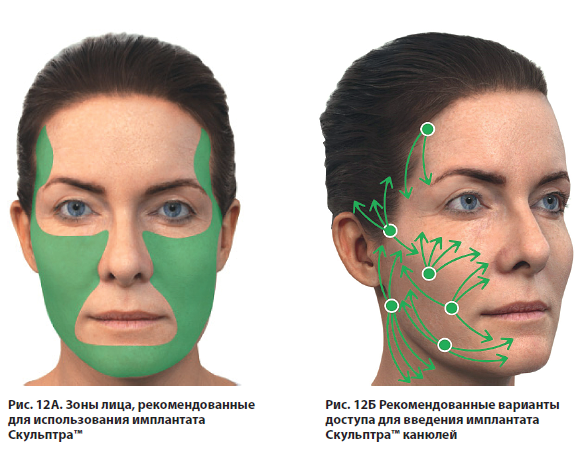
В ряде случаев имплантат вводится в глубокие жировые пакеты лица (ROOF, SOOF, преднадкостничный скуловой жир, пространство Ристоу, глубокий медиальный и латеральный щечный жир) в виде микроболюсов объемом не более 0,2–0,3 мл, что, по мнению всех экспертов, является безопасной техникой.
Массирование области введения для равномерного распределения имплантата является обязательным не только в момент процедуры, но и в последующие 5 дней. Таким образом обеспечивается профилактика появления неровностей и формирования узелков.
Для проведения инъекций используются иглы 26–27G длиной 13–25 мм или канюли 22–23G длиной 38–70 мм. Если игла или канюля забиваются микрочастичками PLLA, не следует прилагать усилия, чтобы ввести продукт, необходимо прервать инъекцию, выйти из тканей и поменять иглу/канюлю. Для сохранения однородности суспензии в течение процедуры необходимо периодически встряхивать шприц.
Перед каждой инъекцией рекомендуется проводить аспирационный тест, чтобы избежать попадания суспензии в сосуды.
При образовании пены внутри шприца следует снять иглу (канюлю), нажатием на поршень удалить пену, и только потом продолжать процедуру.
Суспензию Скульптра™ необходимо вводить медленно, равномерно распределяя ее в тканях. Техника инъекций зависит от целей процедуры и выбранной глубины введения.
При субдермальных инъекциях рекомендуется линейно-ретроградная техника с использованием иглы. Необходимый объем суспензии должен быть равномерно распределен по всей зоне коррекции: в среднем это 0,1–0,2 мл/см².
При использовании канюли продукт вводится в поверхностную жировую клетчатку (ПЖК) линейно-ретроградно, веерно по 0,1–0,2 мл (рис. 12Б).
При инъекциях в глубокие жировые пакеты техника введения — микроболюсная с использованием иглы, при этом объем болюса не более 0,2–0,3 мл, или веерная с использованием канюли 22–23G и введением 0,1–0,2 мл на каждый вектор канюли.
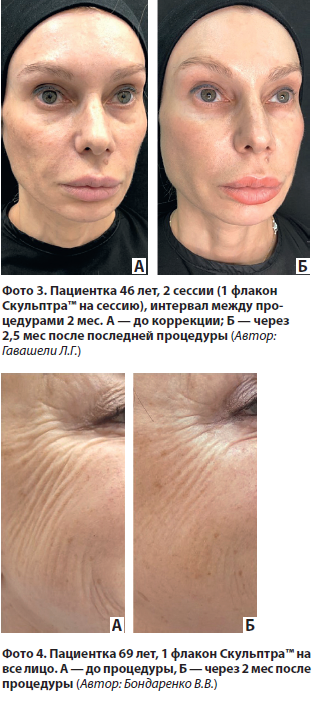
Для пациентов старше 30 лет обычно на курс расходуется примерно 1 флакон препарата на каждые 10 лет возраста. Например, пациентке 40 лет может быть введено 4 флакона на курс, состоящий из 3 сеансов (2, 1 и 1 флакон соответственно). Безусловно, количество сеансов зависит от индивидуальных особенностей пациента и поставленных целей эстетической коррекции. Важно соблюдать оптимальные интервалы между процедурами — не менее 6 нед для одной области [33, 34].
Выбирая место коррекции, следует учитывать толщину тканей и выраженность подкожной жировой клетчатки в разных зонах лица (рис. 13А). Предпочтительные области для подкожного введения: щечно-скуловая, носогубная, нижнечелюстная, подбородочная (рис. 13Б). В височной области имплантат вводится под SMAS между двумя листками поверхностной фасции.
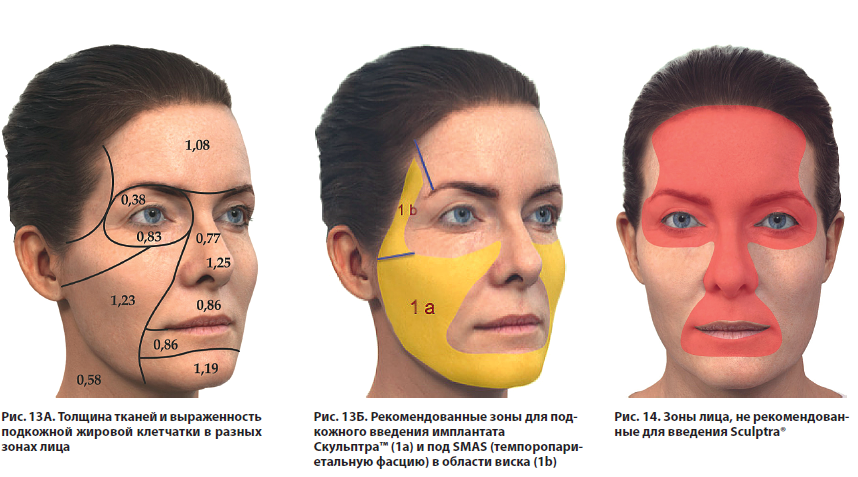
Имплантат Скульптра™ не вводят в зоны высокой мимической активности, в области с тонкой кожей и невыраженной подкожно-жировой клетчаткой, а именно:
- в периорбитальную, включая слезную и веко-щечную борозды;
- периоральную, включая контур и красную кайму губ;
- область лба и глабеллы (межбровная зона);
- нос (рис. 14) [33].
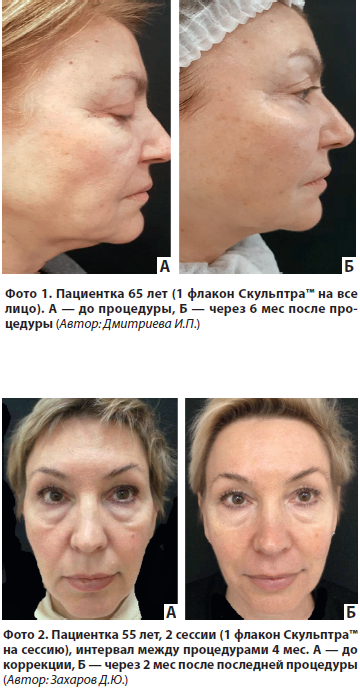
На фото 1–4 представлены клинические примеры.
Нежелательные реакции
Нежелательные реакции от введения имплантата, описанные в инструкции по применению Скульптра™, неспецифичны и сопряжены с самой процедурой инъекции: кратковременное кровотечение в области прокола кожи, преходящая боль в месте инъекции, покраснения, экхимозы, кровоизлияния, легкий отек. Эти явления, как правило (согласно в том числе клиническому опыту российских экспертов), самопроизвольно разрешаются в течение 2–7 дней [17].
Другие нежелательные реакции в основном обусловлены ошибками при приготовлении и/или введении продукта. Характерным элементом некорректного введения имплантата Скульптра™ является узелок. Причиной появления узелков в месте инъекции чаще всего является поверхностное введение, избыточный объем введенного продукта или же его неправильное восстановление, неверно выбранная зона (т.е. зоны со слабо выраженной подкожной жировой клетчаткой: губы, лоб, межбровная зона, кожа над верхней и нижней губой). Также крайне важно проинструктировать пациента о необходимости самомассажа зон инъекции в течение 5 дней после процедуры.
Причиной гиперкоррекции является введение избыточного объема имплантата или применение высококонцетрированной суспензии, еще одна причина — преждевременная повторная коррекция (рис. 15).

Иногда узелки сопровождаются воспалением или изменением пигментации кожи. Раннее появление подкожных узелков в месте инъекции (в течение 6 мес после процедуры) можно минимизировать интенсивным массажем зоны инъекции и «размыванием» частиц PLLA с помощью инъекций 0,9% раствора хлорида натрия. Также целесообразно использование физиопроцедур: ультразвук, фонофорез, электрофорез с препаратами, содержащими ферменты коллагеназы.
В большинстве случаев этих мероприятий достаточно для разрешения узелков. Если вышеприведенных мер недостаточно, можно прибегнуть к хирургическому удалению узелков. Распространенной ошибкой при лечении узелков является применение инъекций глюкокортикостероидов: они не только не помогают в лечении узелков (не путать с гранулемой), но и существенно ухудшают клиническую картину.
Среди других редких нежелательных явлений отметим абсцесс в месте введения, инфекцию в месте введения, склерозирующую гранулему, местную аллергическую реакцию, крапивницу, гипертрофию или атрофию кожи в месте введения, ангионевротический отек, телеангиэктазии, саркоидоз кожи, образование рубцов или изменение пигментации кожи [17].
По данным различных авторов в публикациях до 2006 г., в ответ на введение PLLA (New-Fill®, восстановленный в 3 мл СВДИ) частота появления гранулем инородного тела составляла 0,04–0,1%. Склерозирующие гранулемы появлялись через 6–24 мес после введения и были связаны с интрадермальной имплантацией продукта, высокой концентрацией суспензии, введением имплантата в зоны активной мимики (периорально, периорбитально), приемом медикаментов (интерфероны, антиретровирусные препараты), индивидуальной реактивностью организма пациента.
После изменения протоколов введения, прежде всего концентрации вводимой суспензии, за последние годы нет ни одного сообщения о появлении гранулем после инъекции Скульптра™ (данные из базы международных научных публикаций PubMed и базы сообщений по безопасности компании Galderma) [36].
При лечении гранулем инородного тела (патоморфологическое подтверждение диагноза) российскими экспертами используется наружная терапия препаратами глюкокортикостероидов (бетаметазон, мометазон) и ингибитором кальционеврина в форме мази, фонофорез с глюкокортикостероидами и препаратами, содержащими ферменты коллагеназы, внутриочаговое введение глюкокортикостероидов. При необходимости подключается системная противовоспалительная и иммуносупрессивная терапия.
Профилактика нежелательных явлений на введение имплантата Скульптра™:
- Не использовать высококонцентрированную суспензию — не более чем 1,5–1,8% PLLA (15–18 мг/мл).
- Количество СВДИ на один флакон Скульптра™ должно быть не менее 8 мл.
- Не вводить большой объем продукта в одно место — не более 0,2 мл на 1 см2!
- Не инъецировать продукт интрадермально!
- Недопустимо использовать короткие промежутки между процедурами — менее 6 нед.
- Непосредственно после процедуры проводить интенсивный массаж и пациентам рекомендовать продолжать массировать лицо в последующие 5 дней по 2 мин 2 раза в день.
- Не вводить имплантат в запрещенные зоны: периорбитальную, периоральную, включая контур и красную кайму губ, область лба, глабеллы и носа.
Лечение в случае появления нежелательных реакций
- Болезненность процедуры: предварительная аппликационная анестезия кремом с лидокаином + прилокаином. Непосредственно перед процедурой добавление во флакон с имплантатом Скульптра™ 1–2 мл 2% раствора лидокаина.
- При необходимости после процедуры могут быть однократно назначены внутрь нестероидные противовоспалительные препараты, наружно различные противовоспалительные средства, гель/мазь c арникой и т.д.
- Отечность: рекомендовано применение посттравматических наружных средств (крем-бальзам от синяков и отеков, противовоспалительные средства, гель/мазь c арникой и т.д.). В день процедуры может быть рекомендован антигистаминный препарат на ночь.
- Кровоизлияния, петехии, гематомы: прикладывание холода перед процедурой, после процедуры использование гелей с гепарином, наружных противовоспалительных средств и т.д.
- Узелки, неровности, папулы: интенсивный массаж зон инъекций несколько раз в день, размывание частиц с помощью инъекций 0,9% раствора хлорида натрия, физиопроцедуры: ультразвук, фонофорез, электрофорез с препаратами, содержащими ферменты коллагеназы. Хирургическое удаление при необходимости.
Постпроцедурные мероприятия
После инъекций имплантата Скульптра™ рекомендуется охладить кожу с помощью индивидуальных охлаждающих успокаивающих масок или хладопакетов. Сразу после процедуры необходимо провести тщательный массаж зон инъекции для равномерного распределения имплантата. На завершающем этапе пациенту даются рекомендации об обязательном выполнении самомассажа в домашних условиях (например, с использованием дерматокосметических средств Cetaphil® Физиологического очищающего лосьона или Cetaphil® Восстанавливающего кожу увлажняющего лосьона) по 2 мин 2 раза в день в течение 5 дней после процедуры (рис. 16) [37].

В день процедуры не рекомендуется наносить на кожу декоративную косметику. В течение 5 дней после процедуры следует избегать воздействия прямых солнечных лучей, посещения солярия, сауны, активных физиотерапевтических, косметических процедур. В сезон активного солнца для защиты кожи рекомендуется использовать фотозащитные средства с SPF не менее 30. Важно информировать пациента о том, что имплантат Скульптра™ может визуализироваться при проведении ультразвукового исследования и МРТ, но не определяется при КТ и рентгеновском обследовании [17].
Сочетание с другими эстетическими процедурами
Возможно комбинированное применение инъекций имплантата Скульптра™ с аппаратными и другими методиками эстетической коррекции в соответствии с протоколами.
Если зоны и глубина введения не совпадают, то Скульптра™ может применяться за один визит пациента в комбинации с филлерами, скинбустерами, нейропротеином типа А.
Если после применения имплантата Скульптра™ пациенту планируется проведение сеанса лазерной терапии, химического пилинга и других эстетических процедур, связанных с активным ответом кожи, то существует возможный риск возникновения воспалительной реакции в месте введения имплантата.
Скульптра™ вводится после полного восстановления кожи после таких процедур.
Таблица 1. Рекомендации Российского консенсуса экспертов по применению СкульптраÔ для эстетической коррекции лица (сводная информация)
|
Вопросы к обсуждению |
Рекомендации |
|
Каким пациентам показано применение СкульптраÔ (показания к применению) |
Атония кожи, дряблость, глубокие морщины, складки, потеря объема, липоатрофия, асимметрия |
|
Зоны, не рекомендованные к применению Скульптра™ |
Лоб, губы, нос, периоральная и периорбитальные области и межбровная зона |
|
Число процедур для первичного курса коррекции всего лица |
1–3 |
|
Количество флаконов на одну процедуру при коррекции лица |
1–2 |
|
Интервал между процедурами в неделях |
Не менее 6 |
|
Объем СВДИ для восстановления |
8 мл (дополнительно можно добавить 1–2 мл 2% раствора лидокаина во флакон непосредственно перед введением СкульптраÔ) |
|
Гидратация: необходимый объем и время выдержки |
2–48 ч при комнатной температуре |
|
Игла и/или канюля? |
Игла и/или канюля в зависимости от зоны введения |
|
Размер иглы и/или канюли |
Игла 26–27G длиной 13–25 мм Канюля 22–23G длиной 38–70 мм |
|
Техники введения для коррекции лица |
Линейно-ретроградная, веерная с помощью иглы или канюли, глубокие микроболюсные по 0,1–0,3 мл |
|
Глубина введения |
Субдермально в поверхностные жировые пакеты, в глубокие жировые пакеты |
|
Необходимость массажа во время и после процедуры? Какой режим массажа может быть рекомендован пациентам после процедуры? |
Массаж корректируемой зоны рекомендован во время и сразу после процедуры, далее по 2 мин 2 раза в день на протяжении 5 дней |
|
Когда наблюдается первый эффект от введения продукта при коррекции всего лица? |
Через 4–6 нед с прогрессивным улучшением на протяжении 6 мес |
|
Максимальная длительность эффекта |
1,5–2 года |
|
Когда нужно повторять 2-й курс процедур после завершения 1-го курса? |
Один раз в 1–1,5 года |
|
Возможное применение СкульптраÔ в сочетании с другими методами эстетической коррекции |
Скульптра™ можно применять в комбинации с филлерами, скинбустерами, нейропротеинами типа А, аппаратными методами, нитевым лифтингом и подтяжкой лица, соблюдая безопасные интервалы |
|
Какие меры необходимо предпринимать для безопасного применения продукта? |
· Правильный выбор пациента для коррекции имплантатом Скульптра™ · Детальный сбор анамнеза пациента · Корректное приготовление продукта · Выбор правильной техники введения и плана процедур, включая объем введения (избегать гиперкоррекции) и промежуток между процедурами · Массаж во время и после процедуры · В случае нежелательных побочных реакций проводить своевременные рекомендуемые меры |
Использование имплантата Скульптра™ для коррекции экстрафациальных зон
По мнению международных и российских экспертов, имплантат Sculptra® показан для коррекции дряблости и атонии кожи тела, изменений рельефа, птоза тканей, локальной атрофии после липосакции, а также растяжек и целлюлита [38–40].
Зоны, рекомендованные для использования имплантата:
- шея;
- декольте;
- аксиллярная зона;
- надлоктевая и надколенная зона;
- внутренняя поверхность плеч и бедер;
- живот, ягодицы.
Использование Sculptra® для эстетической коррекции области молочных желез, тыльной поверхности кистей рук, икроножной области и половых органов не рекомендуется ввиду отсутствия данных по безопасности и эффективности, а также положительного опыта применения в этих областях.
Перед началом применения имплантата Скульптра™ важно учитывать следующие аспекты, которые могут повлиять на результат: наличие значительного птоза и избытков кожи, образ жизни, избыточная инсоляция, курение и дефицитное питание, менопауза. Все эти факторы могут привести к снижению индивидуальной реакции организма на инъекцию и потребовать увеличения количества сеансов и/или необходимости увеличения общего объема вводимого имплантата.
Использование имплантата Скульптра™ для эстетической коррекции тела (зоны ниже края нижней челюсти) всегда предполагает дополнительное разведение, большее, как минимум, в 2 раза от стандартного. То есть после предварительного восстановления флакона Скульптра™ в 8 мл стерильной воды для инъекций (СВДИ) непосредственно перед инъекцией к суспензии добавляют 2 мл 2% раствора лидокаина и 6–10 мл СВДИ, таким образом конечный объем суспензии составляет 16–20 мл.
Концентрация PLLA при общем объеме суспензии 20 мл составляет 0,75% (7,5 мг/мл).
Для смешивания удобно использовать шприц 20 мл для аспирации 8 мл суспензии из флакона, 2 мл 2% раствора лидокаина и 6–10 мл СВДИ. С помощью стерильного коннектора следует перенести содержимое в меньшие по объему шприцы (1 или 3 мл) для инъекций. Обычно на одном сеансе используют 1 флакон Скульптра™ на область, по площади эквивалентную странице А4. Эта рекомендация справедлива для всех областей тела.
После процедуры необходимо массировать область введения в течение нескольких минут. Пациентам рекомендуют делать массаж этой области по 2 мин 2 раза/день в течение 5 дней после процедуры. Еще одна важная постпроцедурная рекомендация — избегать физической активности в первые 24 ч и пребывания на солнце.
Для лифтинга кожи обычно требуется 2–4 сеанса инъекций имплантата Скульптра™ с интервалами не менее 6 нед. В большинстве случаев первые результаты появляются через 2–3 мес.
Для сохранения эффекта рекомендуются дополнительные сеансы инъекций каждые 12–18 мес в зависимости от степени снижения эластичности кожи.
Область шеи
Особенностью инволюционных изменений в области шеи является возрастное уменьшение тонуса кожи шеи и подподбородочной зоны, увеличение шейно-подбородочного угла, кожный птоз с аккумуляцией подкожного жира и без него, деформация формы шеи, появление или усугубление горизонтальных складок на шее, а также проявление лентиго и мелазмы.
Кожа шеи характеризуется меньшей толщиной и плотностью по сравнению с кожей лица в связи со слабо развитыми структурными составляющими и меньшей плотностью придатков кожи (потовых и сальных желез), что требует более осторожного подхода к коррекции и применения менее агрессивных косметологических методов. Такие изменения кожи шеи, как дегидратация, снижение тургора и эластичности кожи шеи, становятся заметными раньше, чем на коже лица.
В развитии возрастных изменений также большое значение имеют истончение подкожного и подмышечного (под m. platysma) слоев жировой клетчатки и индивидуальные особенности строения подкожной мышцы шеи.
Показаниями для использования имплантата Скульптра™ в области шеи являются:
- горизонтальные глубокие морщины и поперечные морщины в центральной части шеи;
- потеря тонуса кожи, атрофия дермы и подкожных тканей;
- птоз кожи, дряблость.
Для коррекции зоны шеи используется суспензия с низкой концентрацией PLLA — 0,75–0,85% (16–20 мл СВДИ на 1 флакон Скульптра™), при этом чем тоньше кожа, тем ниже должна быть концентрация.
Препарат вводится иглой или канюлей линейно-ретроградно, веерно.
Инъекции делаются на глубину 2–3 мм — в подкожный жировой слой. Визуальные критерии правильной глубины введения: при приподнимании введенной в ткань канюли или иглы она должна контурировать, но не просвечивать.
Рекомендуется использовать иглы 26–27G длиной 13–25 мм и канюли 22–23G длиной 38–50 мм. Плотность введения препарата — 0,1 мл на 1 см2. Количество препарата на одну процедуру составляет от 0,5 до 1 флакона.
После процедуры проводится тщательный массаж зон инъекции и даются рекомендации пациенту об обязательном выполнении самомассажа в домашних условиях 2 раза в день по 2 мин на протяжении 5 дней для равномерного распределения продукта и во избежание его скопления.
Курс эстетической коррекции с помощью Скульптра™ формируется индивидуально в зависимости от возраста пациента и симптомов возрастных изменений шеи. На курс в течение года может понадобиться от 1 до 3 процедур с интервалом между ними не менее 6 нед. Для поддержания результата повторные курсы процедур проводятся 1 раз в 12–18 мес.
Клинические протоколы в зависимости от степени старения (модифицированная шкала морщин по Томасу Фицпатрику) (табл. 2) [41].
Таблица 2. Модифицированная классификация морщин по Томасу Фицпатрику
|
Класс |
Тип морщин |
|
I |
A. Поверхностные мимические морщины B. Мимические и поверхностные статические морщины C. Мимические и поверхностные статические морщины, начальные изменения текстуры кожи |
|
II |
A. Мимические и статические морщины средней степени выраженности, начальные изменения текстуры кожи B. Глубокие мимические, статические морщины средней степени выраженности на фоне изменения структуры кожи |
|
III |
A. Глубокие мимические, статические средние и глубокие, выраженные изменения текстуры кожи B. Глубокие мимические, статические средние, выраженные изменения текстуры кожи, незначительные избытки кожи |
- Класс 1: Поверхностные статические морщины, начальные изменения кожи.
Рекомендовано: 1 процедура, 1 флакон Скульптра™, оценка результата через 2–3 мес. - Класс 2: Статические морщины средней степени выраженности, начальные изменения текстуры кожи.
Рекомендовано: 2 процедуры по 1 флакону Скульптра™ с интервалом 2–3 мес. - Класс 3: Статические средние и глубокие морщины, выраженные изменения текстуры кожи, незначительный избыток кожи. Рекомендовано: 3 процедуры по 1 флакону Скульптра™ с интервалом 2–3 мес.
При отборе пациентов для процедуры инъекций имплантата Скульптра™ в области шеи, кроме общих противопоказаний, указанных выше, следует избегать введения имплантата пациентам, имеющим выраженные локальные жировые отложения в субментальной зоне и значительную степень птоза тканей.
При дегидратации и атонии дермы с выраженными атрофическими изменениями требуется предварительная «позитивная стимуляция» (например, cкинбустерами Restylane® Vital Light).
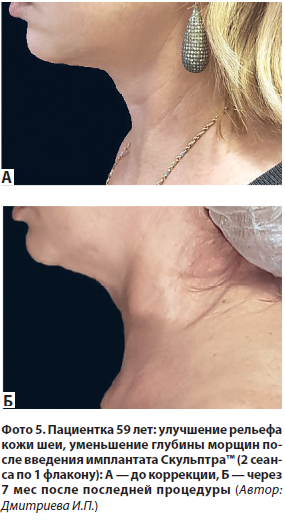
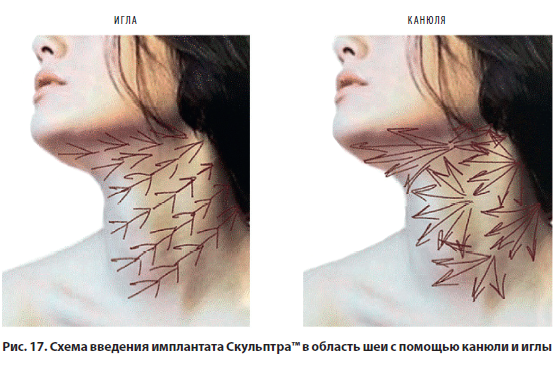
Схема введения имплантата Скульптра™ в область шеи с помощью иглы и канюли представлена на рис. 17. Клинический пример приведен на фото 5.
Область декольте
Процесс старения в зоне декольте сопровождается сухостью кожи, изменением ее рельефа, появлением морщин, изменением тонуса, дряблостью, атрофией кожи и подкожных тканей.
Показанием для использования имплантата Скульптра™ является дряблость, атония кожи, статические морщины, атрофия подкожной жировой клетчатки.
НЕ РЕКОМЕНДУЕТСЯ введение PLLA непосредственно в область молочных желез, в связи с тем, что нет достоверных данных о безопасности проведения процедуры в данной зоне.
Способ приготовления суспензии Скульптра™, техники инъекций схожи с таковыми при использовании в области шеи и описаны выше. На одну процедуру в зоне декольте используется 1 флакон имплантата.
Для проведения процедуры используются иглы 26–27G длиной 13–25 мм, канюли 22–23G длиной 50–70 мм.
Уровень введения — верхний уровень гиподермы (3–4 мм).
Клинические протоколы в зависимости от степени старения (модифицированная шкала старения по Томасу Фицпатрику (табл. 2) [41].
- Класс 1: Поверхностные статические морщины, начальные изменения кожи.
Рекомендовано: 1 процедура, 1 флакон Скульптра™, оценка результата через 2–3 мес. - Класс 2: Статические морщины средней степени выраженности, начальные изменения текстуры кожи.
Рекомендовано: 2 процедуры по 1 флакону Скульптра™ с интервалом 2–3 мес. - Класс 3: Статические средние и глубокие морщины, выраженные изменения текстуры кожи, незначительный избыток кожи.
Рекомендовано: 3 процедуры по 1 флакону Скульптра™ с интервалом 2–3 мес.
Для поддержания результата повторные курсы процедур проводятся 1 раз в 12–18 мес.
Техники введения имплантата Скульптра™ в область декольте с помощью иглы и канюли представлены на рис. 18.
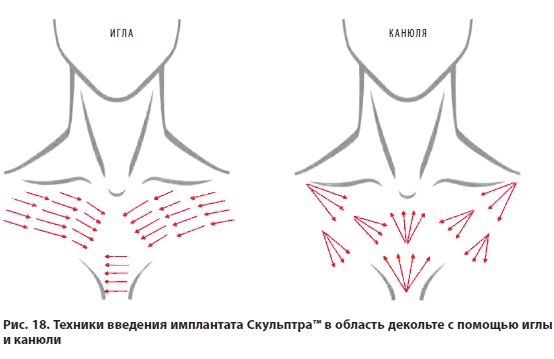
При глубоких межгрудных морщинах и выраженном фотоповреждении кожи декольте возможна техника скретчинг (от англ. to scratch — царапать). Она выполняется с помощью канюли: при ретроградном введении имплантата кончик канюли разворачивается к поверхности кожи и как бы «царапает» кожу изнутри.
Рекомендован массаж сразу после проведения процедуры и в течение 5 дней ежедневно 2 раза в день по 2 мин.
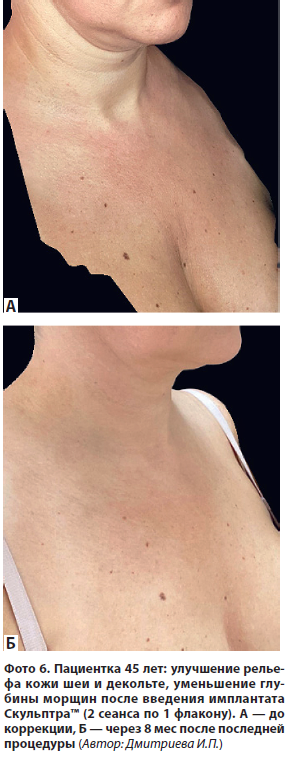
На фото 6 приведен клинический пример.
Живот
На толщину (табл. 3) и на процесс инволюции кожи этой области большое влияние оказывают протекание беременности, гормональные дисфункции, перепады массы тела, послеоперационные рубцы и неровности кожи.
Показаниями для применения имплантата Скульптра™ являются:
- возрастные изменения кожи живота (птоз, атрофия, морщины и складки);
- атрофические полосы (стрии);
- последствия операций, в том числе пластических, когда происходит чрезмерное истончение кожи и подкожной жировой клетчатки (втяжения, неровности кожи).
Таблица 3. Толщина кожи по слоям в области живота [42]
|
Эпидермис, мм |
Дерма, мм |
ПЖК, мм |
|
0,063–0,126 |
1,64–2,32 |
2,18–18,83 |
В области живота используется суспензия с низкой концентрацией PLLA 0,75-0,85% (16–20 мл СВДИ на 1 флакон).
Препарат вводится с помощью иглы 26–27G длиной 13–25 мм или канюли 21–23G длиной 50–70 мм в подкожную жировую клетчатку. В этом случае игла или канюля свободно двигаются в мягких тканях параллельно поверхности кожи. Такая техника подходит для коррекции дряблости кожи, зон липоатрофии и неровностей, возникших после липосакции.
Для работы с послеоперационными осложнениями в виде втяжений и неровностей кожи можно использовать технику субцизии с помощью канюли 21–22G: она позволяет освободить дно атрофического рубца от соединительнотканных тяжей, идущих через дерму. Выполняется в два этапа: сначала подсечение рубца до момента выравнивания его с поверхностью кожи, затем введение имплантата Скульптра™ в проблемную область.
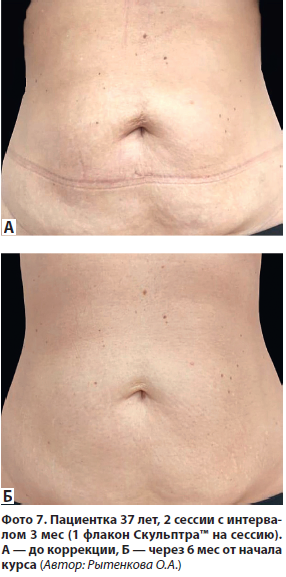 В области выраженной атрофии кожи (стрии, надпупочная зона) дополнительное ведение продукта может быть выполнено субдермально — на границе дермы и гиподермы. Особенность данной техники в том, что при введении иглы или канюли отсутствует их просвечивание через мягкие ткани, в то же время тест на подвижность инструмента в тканях отрицательный, и дерма идет вслед за иглой или канюлей при их покачивании вверх-вниз. Также может быть использована техника скретчинга (см. выше).
В области выраженной атрофии кожи (стрии, надпупочная зона) дополнительное ведение продукта может быть выполнено субдермально — на границе дермы и гиподермы. Особенность данной техники в том, что при введении иглы или канюли отсутствует их просвечивание через мягкие ткани, в то же время тест на подвижность инструмента в тканях отрицательный, и дерма идет вслед за иглой или канюлей при их покачивании вверх-вниз. Также может быть использована техника скретчинга (см. выше).
Курс эстетической коррекции имплантом Скульптра™ формируется индивидуально в зависимости от выраженности изменений кожи. На курс может понадобиться от 2 до 4 процедур с интервалом между ними не менее 6 нед. Количество продукта на одну процедуру составляет 1–2 флакона (1 флакон на верхнюю половину живота и 1 флакон на нижнюю половину живота).
Для поддержания результата может быть использовано меньшее количество имплантата Скульптра™ (0,5–1 флакон на 1 зону) один раз в 12–18 мес.
При отборе пациентов для процедуры коррекции в области живота кроме общих противопоказаний, указанных выше, следует избегать введения имплантата пациентам, имеющим выраженные локальные жировые отложения, с ИМТ более 25 кг/м2 и значительными избытками кожи (кожная складка более 1 см).
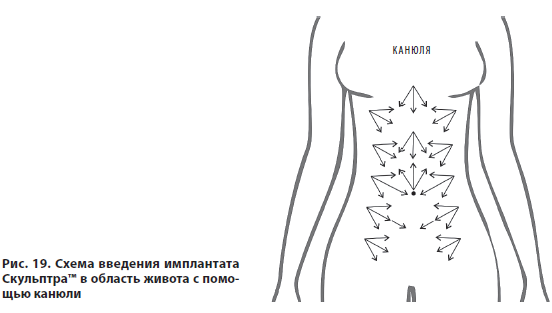
На рис. 19 представлена схема введения Скульптра™ в область живота с помощью канюли. На фото 7 показан клинический пример.
Сгибательная и разгибательная поверхности плеч
Основное показание для использования имплантата Скульптра™ в этих зонах — снижение тонуса и дряблость кожи.
Для успешной коррекции необходим тщательный отбор пациентов. Учитываются данные пликометрии (измерения толщины жировой складки).
- На разгибательной поверхности плеча складка измеряется при опущенной руке в верхней трети плеча в области трехглавой мышцы, ближе к ее внутреннему краю, складка берется вертикально.
- На сгибательной поверхности плеча складка измеряется в верхней трети внутренней поверхности плеча, в области двуглавой мышцы, складка берется вертикально.
При среднем уровне депонирования жира толщина складки составляет 1–3 см; ниже средней — менее 1 см. При толщине складки выше средней, более 3 см, от процедуры с введением имплантата Скульптра™ лучше отказаться.
Также можно учитывать степень птозирования мягких тканей данной области при горизонтальном супинированном отведении руки от туловища (имеется в виду дугообразное провисание ткани по отношению к оси плечевой кости).
Необходимо учитывать общий ИМТ: пациентам с ИМТ более 25 кг/м2 проводить коррекцию не рекомендуется.
Имплантат следует восстанавливать в 16–20 мл СВДИ на 1 флакон, концентрация PLLA в суспензии 0,75–0,85%. Объем введения за 1 сессию — из расчета 1 флакон Скульптра™ (20 мл раствора) на одну конечность, плотность введения — 0,1 мл/см2.
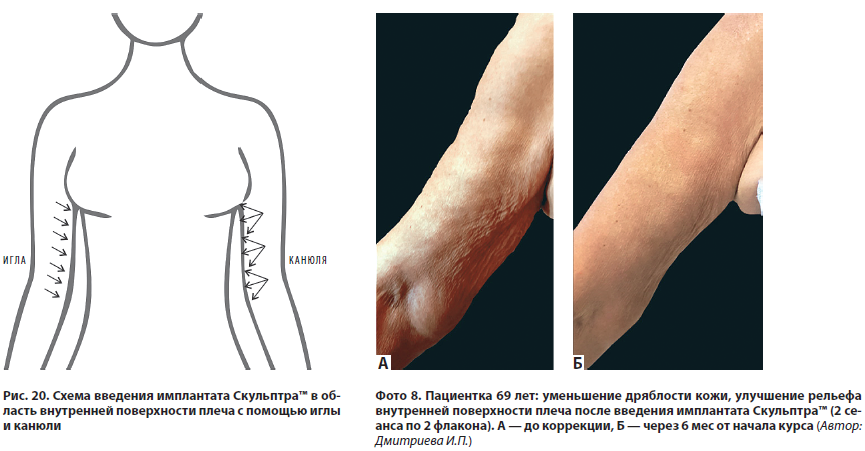
Имплантат вводится субдермально — на границе дермы и гиподермы и в подкожный слой на глубину 4–5 мм линейно-ретроградно, веерно с использованием иглы 26–27G длиной 13–25 мм или канюли 21–23G длиной 50–70 мм (рис. 20). На фото 8 представлен клинический пример.
Аксиллярная зона
Показанием к использованию Скульптра™ в аксиллярной зоне является снижение тонуса, дряблость кожи, образование кожных складок, валиков в области перехода к груди спереди и лопатке сзади.
Оптимальной для коррекции является толщина складки, не превышающая 1 см.
Концентрация препарата и способ приготовления суспензии такой же, как при коррекции разгибательной поверхности рук (описан выше). Количество имплантата Скульптра™ на 1 процедуру — 1 флакон (по 0, 5 мл на каждую сторону).
Имплантат вводится субдермально на границе дермы и гиподермы и в подкожный жировой слой канюлями 21–23G длиной 50–70 мм. Не рекомендовано использование игл, учитывая анатомические особенности строения этой зоны (рис. 21). На фото 9 показан клинический пример.
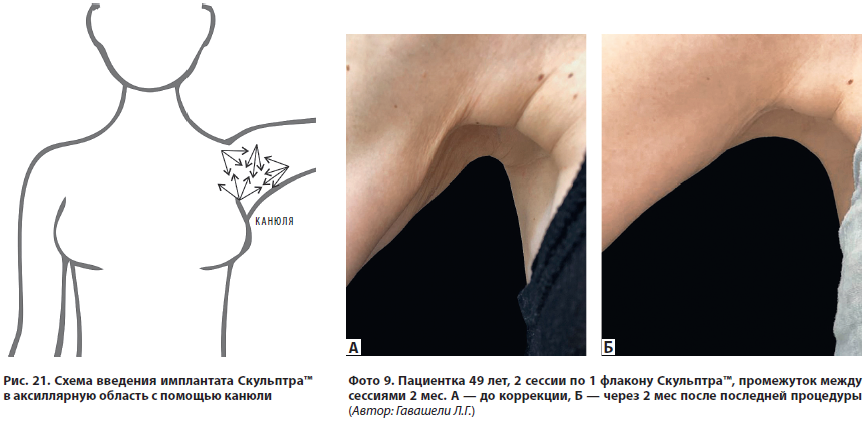
НЕ РЕКОМЕНДУЕТСЯ введение PLLA непосредственно в область молочных желез, в связи с тем, что нет достоверных данных о безопасности проведения процедуры в данной зоне.
Задняя локтевая область
Нависание кожи над локтевым отростком локтевой кости может быть обусловлено возрастной дряблостью кожи из-за снижения содержания коллагеновых волокон, колебаниями веса, значительным похудением, выраженным фотоповреждением кожи. Процедура введения имплантата Скульптра™ эффективна при всех перечисленных состояниях. Исключением является избыточная масса тела (ИМТ более 25 кг/м2) и толщина нависающей складки более 1 см.
Имплантат следует восстанавливать в 16–20 мл СВДИ, концентрация PLLA в суспензии 0,75–0,85%. Объем введения за 1 сессию — 1 флакон продукта, по 0,5 флакона на каждую сторону, плотность введения 0,1 мл/см2.
Скульптра™ вводится субдермально на границе дермы и в подкожный жировой слой. При выполнении процедуры из-за анатомической особенности зоны рекомендованы канюльные техники введения имплантата («перекрестное веерное прошивание») (рис. 22).
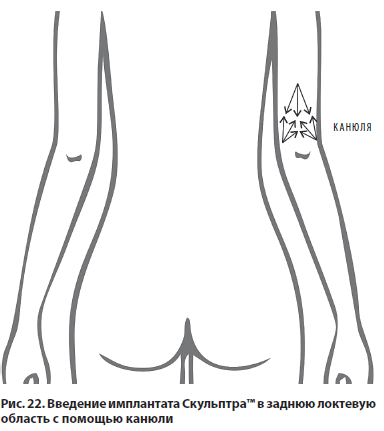
После процедуры рекомендуется провести массаж зоны введения имплантата и рекомендовать пациентам выполнять его в домашних условиях в течение 2 мин 2 раза в день 5 дней.
Таким образом, в зависимости от выраженности изменений кожи в области разгибательной поверхности плеча, аксиллярной и надлоктевой зонах на одну процедуру может быть использовано 4 флакона имплантата Скульптра™ одномоментно.
На курс может понадобиться от 2 до 4 процедур с интервалом между ними не менее 6 нед. Для поддержания результата может быть использовано меньшее количество имплантата (2 флакона) для проведения процедуры один раз в 12–18 мес.
Внутренняя поверхность бедер
Возрастные изменения этой зоны проявляются снижением эластичности и тургора кожного покрова, появлением тонких поверхностных линий и целлюлита. Все это является показанием к коррекции с помощью коллагеностимулятора Скульптра™. Кроме того, к терапевтическим показаниям следует отнести стрии различной степени выраженности, а также неровности рельефа кожи после проведенной липосакции.
На сегодняшний день не существует единой общепринятой шкалы возрастных изменений в области внутренней поверхности бедра. Однако, опираясь на клиническую картину возрастных изменений и изменений контуров тела, Song A.Y. и соавт. выделили 4 стадии птоза согласно так называемой, Питтсбургской шкале [43]:
- 0 — без изменений, не требует лечения;
- 1 — слабая степень выраженности деформации рельефа кожного покрова, требуются минимально инвазивные процедуры;
- 2 — средняя степень выраженности деформации рельефа кожного покрова, возможно хирургическое лечение;
- 3 — тяжелая степень выраженности деформации рельефа кожного покрова, необходима комбинация хирургических и нехирургических методов терапии.
При выборе техники коррекции авторы принимали во внимание индекс массы тела, соотношение вес/рост и зональное распределение подкожной жировой клетчатки в каждом конкретном клиническом случае. Соответственно, к противопоказаниям к проведению инъекционного введения имплантата Скульптра™ следует отнести, в первую очередь, избыточный индекс массы тела (более 30 кг/м2) и значительные избытки кожного покрова в области внутренней поверхности бедра.
Рассматривая технические аспекты проведения процедуры введения имплантата Скульптра™, следует учитывать так называемые линии Лангера. Лангер описал условно проведенные линии на поверхности кожи, вдоль которых она наиболее растяжима. Вдоль линий Лангера прочность кожного покрова выше, как правило, они находятся в местах естественных складок кожи и направлены перпендикулярно мышечным волокнам. Российские эксперты считают целесообразным вводить имплантат Скульптра™, ориентируясь на линии Лангера.
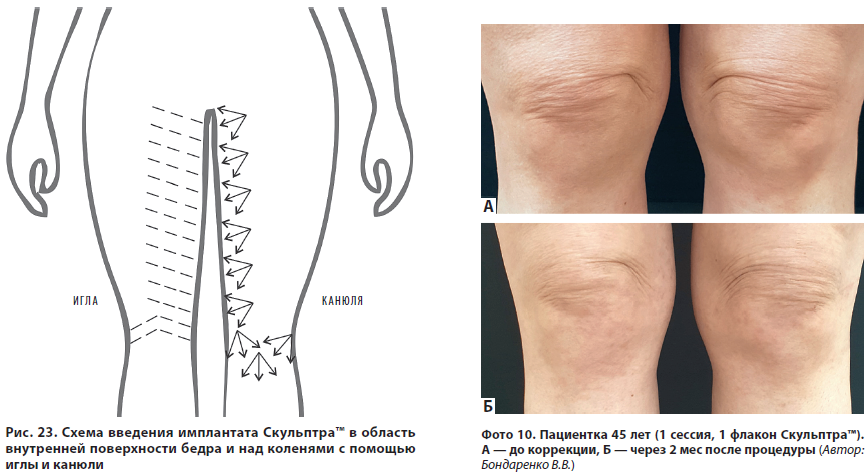
Общий объем СВДИ вместе с 2 мл 2% раствора лидокаина составляет 20 мл на 1 флакон Скульптра™. В этом случае готовая суспензия позволяет проводить коррекцию безопасно и эффективно, что доказано клиническим опытом экспертов. Удается получить результат лифтинга в области медиальной поверхности бедра. Инъекции проводятся игольной либо канюльной техникой с учетом расположения линий Лангера (рис. 23). Для проведения инъекций используются иглы 26–27G длиной 13–25 мм или канюли 21–23G длиной 50–70 мм. Уровень введения имплантата — субдермальный, на глубину 3–4 мм в поверхностный слой подкожной жировой клетчатки (табл. 4). Плотность введения — 0,1 мл/см2. На одну зону (нога) используется 1 флакон продукта, на 2 ноги, соответственно, 2 флакона. На курс может понадобиться от 2 до 4 процедур с интервалом между ними не менее 6 нед. Для поддержания результата может быть использовано меньшее количество имплантата Скульптра™ (1–2 флакона) для проведения процедуры один раз в 12–18 мес.
Таблица 4. Толщина кожи по слоям в области внутренней поверхности бедер [42]
|
Эпидермис, мм |
Дерма, мм |
ПЖК, мм |
|
0,087–0,163 |
2,47–3,06 |
0,62–0,89 |
Надколенная зона
Возрастные изменения в надколенной области чаще всего связаны со снижением эластичности кожи, птозом, локальными жировыми отложениями. Однако анатомические особенности старения коленной области, такие как дегенеративно-дистрофические изменения надколенника, наднадколенникового жирового тела и фиксирующих связок, изменение угла мышечной тяги, принимают непосредственное участие в появлении клинической картины птоза.
К прямым показаниям для коррекции надколенной зоны с помощью препарата Скульптра™ относят, в первую очередь, появление тонких кожных линий и кожной складки средней степени выраженности у пациентов с нормальным ИМТ, неравномерный рельеф кожного покрова в данной области вследствие анатомических особенностей либо после проведения аппаратных процедур и хирургических вмешательств. К противопоказаниям относят наличие избыточного количества подкожной жировой клетчатки локально в этой зоне, ИМТ более 30 кг/м2, значительный птоз кожного покрова и наличие кожной складки толщиной более 1 см.
Для коррекции надколенной зоны препарат Скульптра™ подлежит восстановлению в 20 мл СВДИ на 1 флакон лиофилизата. Для уменьшения субъективных ощущений добавляют 1–2 мл 2% раствора лидокаина. Согласно топологическим линиям Лангера, схема коррекции надколенной области будет соответствовать их расположению. Для введения используются иглы 26–27G длиной 13–25 мм, на глубине 3-4 мм проводятся множественные веерные инъекции (рис. 23). Введение с помощью канюли 21–23G длиной 50–70 мм проводится на такой же глубине, причем чем длиннее канюля, тем меньшее количество точек прокола будет использовано.
Клинические примеры приведены на фото 10.
Ягодицы
Ягодицы — мягкие ткани задней и латеральных поверхностей таза, представленные ягодичными мышцами, подкожной жировой клетчаткой и кожей (табл. 5). Каждая ягодица ограничена сверху областью пояснично-крестцового ромба (ромб Михаэлиса) и крылом подвздошной кости, снизу — подъягодичной складкой и промежностью, а сбоку — областью большого вертела бедра.
Таблица 5. Толщина кожи по слоям в области ягодиц [42]
|
Эпидермис, мм |
Дерма, мм |
ПЖК, мм |
|
0,105–0,209 |
2,33–2,98 |
9,28–23,50 |
Причины птоза ягодиц: генетическая предрасположенность, возрастные изменения в виде атрофии тканей, дряблости, стрий, целлюлита, массивная потеря веса.
Показаниями к использованию имплантата Скульптра™ является гипоплазия ягодиц, липодистрофия, атрофия и дряблость кожи, неровности кожи после липосакции, стрии, целюллитные втяжения, надтрохантерные углубления.
Степень птоза в этой области оценивается по классификации Gonzalez R. (2006 г.) [44], основанной на взаимном расположении двух линий: M — вертикальной срединной линии, Т — вертикальной линии, проходящей через седалищный бугор.
- 0 — нет птоза, складка не пересекает T-линию;
- 1 — легкий прептоз, складка между линиями M и T;
- 2 — средний прептоз, складка достигает M-линии;
- 3 — пограничный прептоз, складка пересекает M-линию, но нет нависания тканей;
- 4 — истинный птоз, нависание тканей над всей ягодичной складкой.
При степени выраженности птоза 0–1 возможна коррекция имплантатом Скульптра™.
При выраженности птоза 2–4-й степени пациентам необходимо предлагать хирургическую коррекцию для получения наглядного результата.
Степень выраженности подкожной жировой клетчатки возможно определить по щипковому тесту:
- Ж0 — толщина складки до 0,5 см;
- Ж1 — толщина кожно-жировой складки 0,5–1,5 см;
- Ж2 — толщина кожно-жировой складки 1,5–2,5 см;
- Ж3 — толщина кожно-жировой складки более 2,5 см.
Чем меньше толщина выраженности подкожной жировой клетчатки, тем большее количество флаконов имплантата Скульптра™ необходимо для проведения успешной коррекции.
Гидратация PLLA производится СВДИ в объеме 16–20 мл.
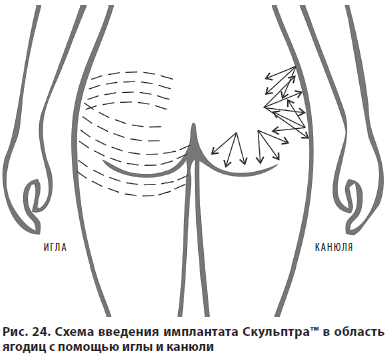
Для коррекции используются иглы 26–27G длиной 13–25 мм и канюли 21–23G длиной 50–70 мм. Техника введения — линейная ретроградная, веерная, перекрестная (рис. 24). Количество флаконов определяется индивидуально: от 2 до 6 за одну сессию.
 Коррекция фиброзных втяжений при целлюлите осуществляется с предварительной субцизией (подсечением) и последующим введением имплантата Скульптра™ в объеме 1–2 флакона за одну сессию.
Коррекция фиброзных втяжений при целлюлите осуществляется с предварительной субцизией (подсечением) и последующим введением имплантата Скульптра™ в объеме 1–2 флакона за одну сессию.
Глубина введения:
- граница дермы и гиподермы — при коррекции дряблости кожи, птоза;
- субдермальный — при коррекции стрий и целлюлита;
- подкожная жировая клетчатка на глубине 1–2 см — для увеличения объема ягодиц, коррекции надтрохантерных углублений и птоза.
После процедуры рекомендуется выполнить массаж зоны введения имплантата с его продолжением в домашних условиях (по 2 мин 2 раза в день 5 дней).
На курс может понадобиться 2–4 процедуры с интервалом между ними не менее 6 нед. Для одного сеанса потребуется 2–6 флаконов. Для поддержания результата может быть использовано меньшее количество имплантата Скульптра™ (2 флакона), процедура проводится 1 раз в год.
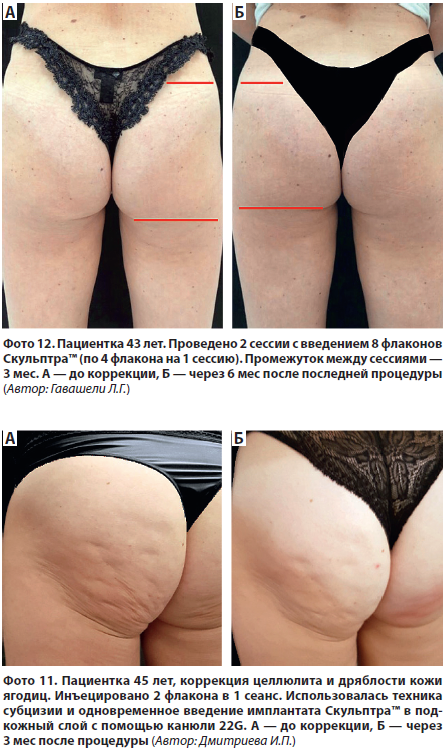
На фото 11, 12 представлены клинические примеры.
Заключение
Скульптра™ — известный и хорошо изученный имплантат-биостимулятор, который действует в глубоких слоях кожи, стимулирует естественную выработку коллагена, таким образом восстанавливая внутреннюю структуру кожи и повышая ее плотность.
Скульптра™ открывает новые возможности для коррекции процессов, связанных со старением тканей не только лица, но и тела (шеи, декольте, внутренней поверхности рук и ног, коленей, живота, ягодиц).
Процедуры с имплантатом Скульптра™ являются малоинвазивными, а формируемый результат долгосрочным (до 25 мес).
Правильный выбор пациента и зоны коррекции ведут к успеху и высокой удовлетворенности процедурой эстетической коррекции с использованием имплантата Скульптра™. Также немаловажно правильное приготовление продукта, в частности его восстановление. Выбор техники введения и составление корректного плана процедур позволяют избежать нежелательных явлений. Равномерное распределение продукта за счет массажа во время и после процедуры — необходимое условие получения естественного результата.
В заключение хочется отметить, что стимуляция неоколлагеногенеза для восстановления объема и биомеханических свойств мягких тканей — это очень перспективный метод коррекции возрастных изменений. Современные концепции и стратегии омоложения направлены не на коррекцию конкретной морщины, а на восстановление гармоничного облика лица и тела в целом, улучшение качества кожи и возвращение ей здорового, моложавого вида. Большинство пациентов заинтересовано в методиках, которые дают длительные результаты. Использование имплантата Скульптра™ как в качестве монотерапии, так и в комбинации с другими методами эстетической коррекции позволяет достойно ответить на эти вызовы времени.
Статья опубликована в журнале «Инъекционные методы в косметологии» №2-2020
На правах рекламы
Литература
- Humble G., Mest D. Soft tissue augmentation using Sculptra. Facial Plastic Surg 2004; 20(2): 157–163.
- Sculptra®, Product Instructions for Use, Dermik Laboratories, USA, 2004. https://www.accessdata.fda.gov/cdrh_docs/pdf3/P030050c.pdf
- Регистрационное удостоверение на медицинское изделие Скульптра™ № ФСЗ 2009/05553 от 03.04.2017.
- Donofrio L.M. Fat distribution: a morphologic study of the aging face. Dermatol Surg 2000; 26(12): 1107–1112.
- Zimbler M.S., Kokoska M.S., Thomas J.R. Anatomy and pathophysiology of facial aging. Facial Plаst Surg Clin North Am 2001; 9(2): 179–187.
- Vleggaar D., Fitzgerald R. Dermatological implications of skeletal aging: a focus on supraperiosteal volumization for perioral rejuvenation. J Drugs Dermatol 2008; 7(3): 209–220.
- Marwah M., Tandon N.S. Pathophysiology of Aging Skin. In: ACS(I) Textbook on Cutaneous & Aesthetic Surgery. Wenkataram M., ed. Jaypee Brothers Medical Publishers, 2012.
- Talwar A., Setty R.D. Cosmeceuticals. In: ACS(I) Textbook on Cutaneous & Aesthetic Surgery. Wenkataram M., ed. Jaypee Brothers Medical Publishers, 2012.
- Ascher B., Coleman S., Alster T., et al. Full scope of effect of facial lipoatrophy: A framework of disease understanding. Dermatol Surg 2006; 32(8): 1058–1069.
- Aesthetic Plastic Surgery National Data Bank Statistics for 2019. https://www.surgery.org/media/statistics
- Bailey A.J., Paul R.G., Knott L. Mechanisms of maturation and ageing of collagen. Mech Ageing Dev 1998; 106(1–2): 1–56.
- Ladislas R. An original approach to ageing: an appreciation of Fritz Verzar’s contribution in the light of the last 50 years of gerontological facts and thinking. Gerontol 2006; 52(5): 268–274.
- Северин Е.С., Алейникова Т.Л., Осипов Е.В., Силаева С.А. Биологическая химия. М.: Медицинское информационное агентство, 2008. 364 с.
- Di Lullo A., Sweeney S.M., Korkko J., et al. Mapping the ligand-binding sites and disease-associated mutations on the most abundant protein in the human, type I collagen. J Biol Chem 2002; 277(6): 4223–4231.
- Fisher G.j., Varani J., Voorhees J.J. Looking older: fibroblast collapse and therapeutic implications. Arch Dermatol 2008; 144(5): 666–672.
- Goldberg D., Guana A., Volk A., et al. Single-arm study for the characterization of human tissue response to injectable poly-L-lactic acid. Dermatol Surg 2013; 39(6): 915–922.
- Инструкция по применению медицинского изделия имплантата для подкожного введения Скульптра™ (поли-L-молочная кислота), 2014.
- Овчинников Ю. А. Биоорганическая химия. М.: Просвещение, 1987, с. 27–36.
- Narins R.S., Baumann L., Brandt F.S., et al. A randomized study of the efficacy and safety of injectable poly-L-lactic acid vs human-based collagen implant in the treatment of nasolabial fold wrinkles. J Am Acad Dermatol 2010; 62(3): 448–462.
- Vleggaar D., Bauer U. Facial enhancement and the European experience with Sculptra™ (Poly-l-lactic Acid). J Drugs Dermatol 2004; 3(5): 542–547.
- Woerle B., Hanke C.W., Sattler G. Poly-L-lactic acid: A temporerty filler for soft tissue augmentation. J Drugs Dermatol 2004; 3(4): 385–389.
- Vleggaar D. Facial volumetric correction with injectable PLLA. Dermatol Surg 2006; 31(11 Pt 2): 1511–1518.
- Mainil-Varlet P., Gogolewski S., Nieuwenhuis P. Long-term soft tissue reaction to various polylactides and their in vivo J Mater Sci Mater Med 1996; 7: 713–721.
- Gogolewski S., jovanovic M., Perren S.M., et al. Tissue response and in vivo degradation of selected polyhydroxyacids: Polylactides (PLA), poly(3-hydroxybutyrate) (PHB), and poly (3- hydroxybutyrate-co-3-hydroxyvalerate) (PHB/VA). J Biomed Mater Res 1993; 27(9): 1135–1148.
- Fitzgerald R., Vleggar D. Facial volume restoration of the aging face with poly-L-lactic acid. Dermatol Ther 2011; 24(1): 2–27.
- Stein Ph., Vitavska O., Kind P., et al. The biological basis for poly-L-lactic acid-induced augmentation. J Dermatol Sci 2015; 78(1): 26–33.
- Mest D.R., Humble G. Safety and efficacy of poly-L-lactic acid injections in persons with HIV-associated lipoatrophy: The US Experience. Dermatol Surg 2006; 32(11): 1336–1345.
- Kulkarni K.P., Pani K.C., Neuman C., et al. Polylactic acid for surgical Implants. Arch Surg 1966; 93(5): 839–843.
- US Food and Drug Administration. PMA P030050/S2 FDA Summary of Safety and Effectiveness Data. US Food and Drug Administration, 2009.
- Sculptra®, Product Labeling, Instructions for Use. Galderma Laboratories, L.P. Fort Worth, Texas, September 2014.
- US Food and Drug Administration. PMA P030050 FDA Summary of Safety and Effectiveness Data, US Food and Drug Administration, 2004.
- Moyle G.C., Lysakova L., Brown S., et al. A randomized open-label study of immediate vs delayed polylactic acid injections for the cosmetic management of facial lipoatrophy in persons with HIV infection. HIV Medicine 2004; 5(2): 82–73.
- Alessio R., Rzany B., Eve L., et al. European expert recommendations on the use of injectable poly-L-lactic acid for facial rejuvenation. J Drugs Dermatol 2014; 13(9): 1057–1066.
- Vleggaar D., Fitzgerald R., Lorenc Z.P., et al. Consensus recommendations on the use of injectable poly-L-lactic acid for facial and nonfacial volumization. J Drugs Dermatol 2014; 13(4 Suppl): 44–51.
- Baumann K., et al. Physicochemical analyses of poly-L-lactic acid reconstituted with immediate use, IMCAS 2020.
- Galderma Data on file.
- Palm M., Chayavichitsilp P. The skinny on Sculptra: a practical primer to volumization with PLLA. J Drugs Dermatol 2012; 11(9): 1046–1052.
- Jabbar A., Arruda S., Sadick N. Off face usage of poly-L-lactic acid for body rejuvenation. J Drugs Dermatol 2017; 16(5): 489–494.
- Haddad A., Menezes A., Guarnier Ch., et al. Recommendations on the use of injectable poly-L-lactic acid for skin laxity in off-face areas. J Drugs Dermatol 2019; 18(9): 929–935.
- Wilkerson E.C., Goldberg D.J. Poly-L-lactic acid for the Improvement of photodamage and rhytids of the dé J Cosmet Dermatol 2018; 17(4): 606–610.
- Shoshani D., Markovitz E., Monstrey S.J., et al. The modified Fitzpatrick Wrinkle Scale: a clinical validated measurement tool for wrinkle severity assessment. Dermatol Surg 2008; 34(suppl 1): 85–91.
- Елисеев Ю.Ю. Заболевания кожи. Полный справочник. М.: Эксмо, 2009.
- Song A.Y., Jean R.D., Hurwitz D.J., et al. A Classification of contour deformities after bariatric weight loss: the Pittsburgh rating scale. Plast Reconstr Surg 2005; 116(5): 1535–1544.
- Gonzalez R. Etiology, definition, and classification of gluteal ptosis. Aesthetic Plast Surg 2006; 30(3): 320–326.




